Introduzione
L’ipertensione è il fattore di rischio più prevalente per la mortalità e gli anni di vita corretti per la disabilità1 in tutto il mondo. Le malattie cardiovascolari rimangono la principale causa di morte a livello globale, con 17,7 milioni di decessi nel 2015, che rappresentano il 31% di tutti i decessi nel mondo.2 L’ipertensione è un fattore importante nelle malattie cardiovascolari.3 Nel 2010 è stato stimato che un terzo della popolazione adulta mondiale soffriva di ipertensione.4 L’introduzione delle linee guida sull’ipertensione dell’American College of Cardiology e dell’American Heart Association nel 2017 ha portato a stime più elevate del numero di persone affette da ipertensione.5,6 La conoscenza dei farmaci antipertensivi di prima linea ottimali per la prevenzione degli eventi cardiovascolari e della mortalità sarà importante per il processo decisionale clinico. Inoltre, l’identificazione dei trattamenti più efficaci per il controllo dell’ipertensione e dei successivi eventi cardiovascolari e della mortalità e che hanno gli effetti meno dannosi è indispensabile per guidare i medici e ridurre il carico di malattie cardiovascolari in tutto il mondo.
Le precedenti meta-analisi hanno esaminato l’efficacia dei trattamenti antiipertensivi nella riduzione degli eventi cardiovascolari.7,8 Queste meta-analisi hanno utilizzato confronti a coppie di sole 2 classi di farmaci antiipertensivi; tuttavia, la meta-analisi a coppie non consente il confronto di più classi di farmaci. Solo 1 meta-analisi di rete9 ha confrontato l’efficacia di diverse classi di farmaci antiipertensivi nella prevenzione degli eventi cardiovascolari, ma questa meta-analisi è stata pubblicata più di 15 anni fa e comprendeva farmaci, come gli α-bloccanti, che sono meno frequentemente utilizzati nell’assistenza sanitaria contemporanea.
Per fornire una prospettiva aggiornata sull’efficacia comparativa dei farmaci antiipertensivi, abbiamo condotto una meta-analisi in rete per confrontare gli effetti riportati di diverse classi di farmaci antiipertensivi attualmente utilizzati per ridurre il rischio di singoli eventi cardiovascolari (morte cardiovascolare, infarto del miocardio, ictus e rivascolarizzazione) e per esaminare l’efficacia dei farmaci riportati nel ridurre il rischio complessivo di qualsiasi evento cardiovascolare. I risultati di questo studio saranno rilevanti per la gestione clinica contemporanea dell’ipertensione, soprattutto alla luce delle nuove linee guida dell’American College of Cardiology e dell’American Heart Association sull’ipertensione.10
Metodi
Abbiamo condotto una meta-analisi in rete di studi clinici randomizzati che hanno testato farmaci antiipertensivi. Questo studio ha seguito le linee guida Preferred Reporting Items for Systematic Reviews and Meta-analyses (PRISMA) per le revisioni sistematiche e le meta-analisi.11
Fonti dei dati e selezione degli studi
Abbiamo cercato sistematicamente nelle banche dati di PubMed, Embase e Cochrane Library gli articoli pubblicati tra il 1° gennaio 1990 e il 24 ottobre 2017. I termini di ricerca utilizzati comprendevano l’ipertensione, l’ipertensione e gli agenti e gli agenti antipertensivi (un elenco dettagliato dei termini di ricerca è disponibile nei metodi eMethods del supplemento. Non vi erano restrizioni linguistiche.
Abbiamo incluso studi che soddisfano i seguenti criteri: (1) studi clinici randomizzati; (2) pubblicati durante o dopo il 1990; (3) inclusi adulti non incinti di 18 anni o più senza malattie renali croniche, nefropatie diabetiche o trapianti d’organo (che sono fattori di rischio per l’ipertensione secondaria) e senza infarto del miocardio e/o ictus nei 6 mesi precedenti; (4) farmaci antiipertensivi valutati, compresi gli inibitori dell’enzima di conversione dell’angiotensina (ACE), calcioantagonisti diidropiridinici (DH CCB), calcioantagonisti non diidropiridinici (nonDH CCB), β-bloccanti, bloccanti del recettore dell’angiotensina (ARB) e diuretici rispetto ai gruppi di controllo che ricevono placebo, trattamento standard o educazione sanitaria; (5) ha riportato l’incidenza di eventi di malattie cardiovascolari (morte cardiovascolare, infarto del miocardio, ictus e/o rivascolarizzazione coronarica [intervento coronarico percutaneo o innesto di bypass coronarico]); e (6) ha riportato dati di almeno 6 mesi di follow-up. Inoltre, abbiamo escluso gli studi che hanno riportato infarto del miocardio e/o ictus nei 3 mesi precedenti; studi che si sono concentrati su pazienti con malattie renali croniche, nefropatie diabetiche o trapianti d’organo (che sono fattori di rischio per l’ipertensione secondaria); e studi che non si sono concentrati su pazienti con ipertensione. Per ridurre al minimo le preoccupazioni circa l’eterogeneità dell’accertamento dell’esito degli studi, abbiamo incluso solo studi in cui gli eventi cardiovascolari sono stati giudicati dai medici utilizzando criteri simili e valutando le cartelle cliniche dei pazienti.
La selezione dello studio è avvenuta in 3 fasi. In primo luogo, 2 di noi (J.W. e A.J.K.) hanno vagliato autonomamente i titoli degli studi. In secondo luogo, gli stessi 2 revisori hanno vagliato e selezionato gli abstract, e i disaccordi sono stati risolti da un terzo revisore (M.K.A.). In terzo luogo, i due revisori (J.W. e A.J.K.) hanno esaminato il testo completo degli articoli per la conferma dell’inclusione. I disaccordi sono stati risolti per consenso o, se necessario, dal terzo revisore (M.K.A.).
Estrazione dei dati e valutazione della qualità
Due di noi (J.W. e A.J.K.) hanno estratto in modo indipendente i dati da studi che soddisfacevano i criteri di inclusione utilizzando un modulo di estrazione standardizzato. I dati estratti includevano la dimensione del campione, le caratteristiche dei partecipanti (età e sesso), il paese dello studio, la durata del follow-up, i tipi di farmaci antiipertensivi e i gruppi di confronto, e il numero di casi al primo esame per ogni risultato.
La morte cardiovascolare è stata definita come la morte legata a malattie cardiovascolari o la morte che può essere calcolata utilizzando la mortalità di tutte le cause meno la morte non cardiovascolare. Abbiamo usato l’infarto miocardico non fatale e l’ictus se erano indicati o potevano essere calcolati, e abbiamo usato l’infarto miocardico totale (fatale e non fatale) e l’ictus come risultati se il numero di infarto miocardico non fatale e di ictus non poteva essere derivato. La rivascolarizzazione comprendeva qualsiasi intervento coronarico percutaneo o innesto di bypass coronarico riportato negli studi clinici. Gli eventi cardiovascolari complessivi sono stati calcolati come aggregazione di morte cardiovascolare, infarto miocardico, ictus e rivascolarizzazione.
Abbiamo valutato la qualità degli studi inclusi utilizzando la scala di Jadad,12 che misura la qualità metodologica degli studi clinici randomizzati su una scala da 0 a 5, con 0 che indica una qualità molto bassa e 5 che indica una qualità rigorosa. Questa scala valuta il rischio di bias sulla base di 3 domini: randomizzazione (inclusa la menzione della randomizzazione e del metodo appropriato di randomizzazione), cecità (inclusa la menzione del cecità e del metodo appropriato di randomizzazione), e considerazione di tutti i pazienti (cioè, i risultati di tutti i pazienti nello studio clinico sono noti e, se non vengono riportati dati, viene indicata la ragione per cui mancano i dati). Ad uno studio potrebbe essere assegnato un massimo di 2 punti ciascuno per i domini di randomizzazione e cecità e 1 punto per il dominio di considerazione di tutti i pazienti, per un possibile punteggio massimo di 5. Due di noi (J.W. e A.J.K.) hanno condotto la valutazione della qualità e assegnato i punteggi di qualità (misura continua) per ogni studio. Gli studi con un punteggio di 3 o più punti sono stati considerati a basso rischio di distorsione, mentre gli studi con un punteggio inferiore a 3 punti sono stati considerati ad alto rischio di distorsione.
Sintesi e analisi dei dati
L’analisi è stata condotta da ottobre 2017 a dicembre 2019. Abbiamo prima condotto una meta-analisi a coppie di studi placebo-clinici per stimare l’effetto diretto sulla riduzione degli eventi cardiovascolari segnalati per ogni agente rispetto al placebo. La differenza di rischio (per 1000 persone) e i numeri necessari per il trattamento sono stati calcolati per ogni tipo di farmaco.
Abbiamo condotto una frequente meta-analisi di rete con modelli ad effetti casuali per stimare le riduzioni aggregate degli eventi cardiovascolari e la rivascolarizzazione per ogni tipo di farmaco antipertensivo rispetto al placebo e tra di loro.13 Abbiamo utilizzato il software Stata, versione 14.0 (StataCorp), per tutte le analisi con il comando di rete.14 Questo approccio è un’estensione del metodo proposto da DerSimonian e Laird,15 e le prestazioni di questo modello sono state soddisfacenti. Il modello contiene una componente di varianza di incoerenza, che è fonte di variazione oltre che di eterogeneità tra gli studi.16 Abbiamo riportato i rapporti di rischio (RR) e i corrispondenti IC al 95%, e abbiamo calcolato un RR e un IC al 95% in pool per ogni gruppo di intervento separatamente da ogni gruppo placebo.
Per ogni classe di farmaci, abbiamo valutato l’eterogeneità tra gli studi utilizzando il metodo della massima probabilità.16 Abbiamo esaminato l’entità di una varianza di eterogeneità comune per la rete (τ 2) come indicatore del grado di eterogeneità tra gli studi inclusi in termini di gamma di stime di trattamento attese (RRs e 95% di ICs). Qualsiasi τ 2 valori inferiori a 0,25 sono stati considerati eterogeneità accettabile; valori compresi tra 0,25 e 1,0 rappresentavano un’eterogeneità moderatamente elevata; e valori superiori a 1,0 rappresentavano un’eterogeneità molto elevata.
Abbiamo valutato l’incoerenza generale all’interno della rete tra gli effetti diretti (confronto tra agenti specifici e placebo) e i confronti indiretti (confronti diversi da quelli diretti all’interno di ogni risultato) per ogni risultato utilizzando i test χ 2. Se non è stata rilevata alcuna incongruenza generale, l’incongruenza tra ciascuno dei 2 agenti è stata testata calcolando le differenze tra gli effetti diretti e i confronti indiretti utilizzando le loro SE.17,18 Abbiamo considerato le prove di incoerenza se i valori di P erano inferiori a .05. Abbiamo valutato le potenziali distorsioni di pubblicazione ispezionando la simmetria dei grafici ad imbuto per ogni risultato.19
Abbiamo condotto analisi di metaregressione per esaminare la relazione dose-risposta tra ogni riduzione di 10 mm Hg di pressione sistolica e 5 mm Hg di pressione diastolica (indipendentemente dai gruppi di intervento) nel tempo e per valutare l’incidenza degli eventi cardiovascolari (compresi i tipi complessivi e individuali di eventi cardiovascolari, con i log RR degli eventi cardiovascolari come variabili dipendenti). Il coefficiente di metaregressione è stato ponderato per 1 diviso per la somma di σ i2 e τ 2, con σ i2 che rappresenta il SE dell’effetto stimato nel particolare studio clinico e con τ 2 che rappresenta la varianza tra studi.20 Inoltre, tra gli studi con informazioni disponibili, abbiamo riportato i tassi di effetti avversi, come edema, cefalea, tosse e ipotensione o vertigini, che sono associati a farmaci antipertensivi e placebo.
Risultati
La nostra ricerca sistematica ha prodotto 4933 articoli (Figura 1). Abbiamo identificato altri 71 articoli da bibliografie di relazioni e recensioni pertinenti. In totale, la revisione sistematica e la meta-analisi della rete hanno incluso 47 articoli pubblicati da 46 studi clinici, con 248-887 partecipanti e 28-658 eventi cardiovascolari al primo tentativo. A causa dell’esiguo numero di studi che riportavano diverse permutazioni di combinazioni di farmaci e CCB non-DH, non abbiamo riportato i dati per i farmaci combinati a dosaggio fisso antipertensivi nella meta-analisi di rete.
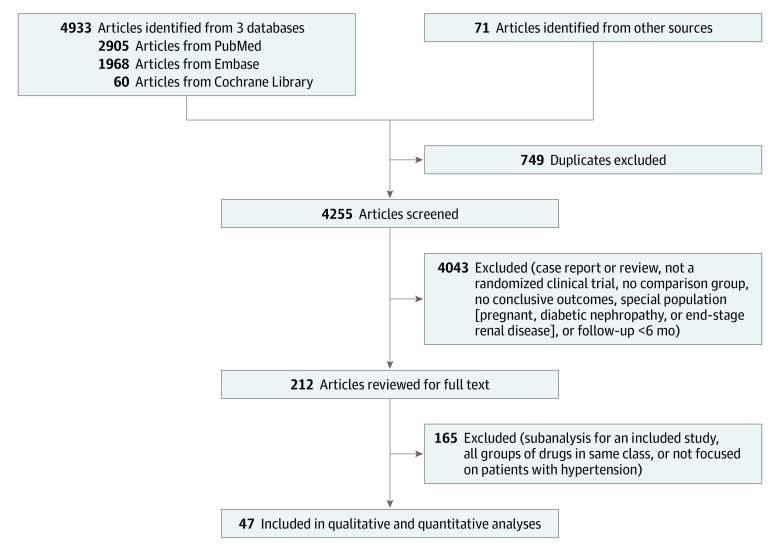
Figura 1.Diagramma PRISMA di ricerca e selezione della letteraturaI motivi di esclusione non sono stati categorizzati per singolo articolo perché ogni articolo può aver soddisfatto più criteri di esclusione.
La Figura 2 mostra il diagramma di rete che illustra le diverse classi di farmaci antipertensivi e i confronti testati. Tra gli studi inclusi, 15 ACE inibitori testati, 23 DH CCB testati, 4 CCB non-DH testati, 8 β-bloccanti testati, 12 ARB testati e 13 diuretici tiazidici testati. Quattro studi provenivano dal Nord America, 18 dall’Europa, 16 dall’Asia, 1 dall’Oceania e 7 da diverse regioni di diversi continenti.
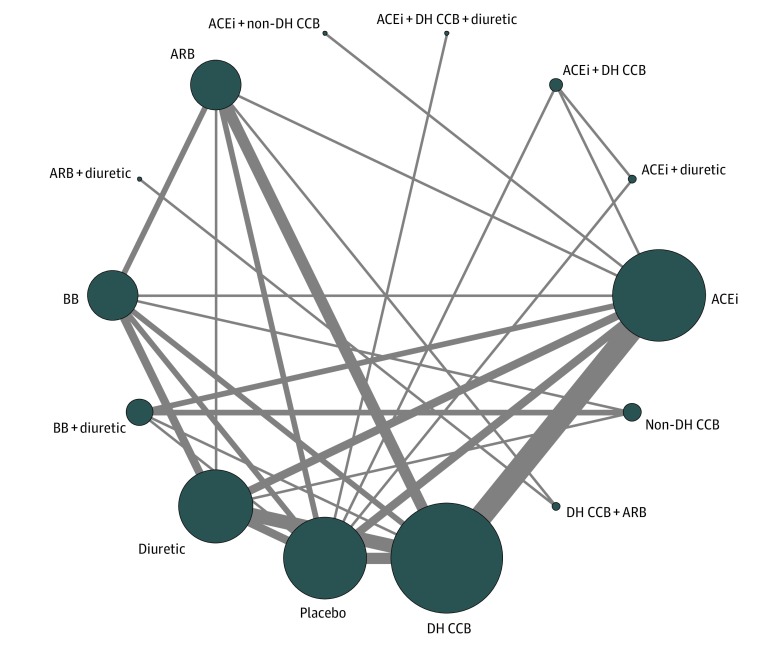
Figura 2.Trama di rete di farmaci antiipertensivi ACEi indica l’inibitore dell’enzima di conversione dell’angiotensina; ARB, bloccante del recettore dell’angiotensina; BB, β-bloccante; DH CCB, calcioantagonista diidropiridinico; e non-DH CCB, calcioantagonista nondiidropiridinico.
L’età media (SD) dei partecipanti era di 65,6 (5,8) anni (range, 51,8-83,8 anni), e il 52,8% (range, 28,2%-100,0%) erano uomini. La pressione sistolica di base media (SD) era di 161,3 (13,6) mm Hg (range, 129-195 mm Hg). Un totale di 14 studi ha incluso il placebo, l’educazione sanitaria, o l’educazione convenzionale nei loro gruppi di controllo, e 35 studi hanno riportato confronti diretti del trattamento (3 dei quali includevano il placebo e 2 agenti di trattamento). Il tempo medio di follow-up (SD) è stato di 3,7 (1,5) anni (range, 1,0-10,0 anni). In tutti gli studi clinici inclusi con particolari classi di farmaci antiipertensivi, la frequenza di utilizzo per ogni tipo di farmaco antiipertensivo è stata simile tra gli studi, con l’età media dei partecipanti sopra e sotto i 65 anni. Per regione di studio, gli ACE inibitori, i β-bloccanti e i diuretici sono stati usati più frequentemente in Europa, i DH CCB sono stati usati più frequentemente in Asia e in Europa, e gli ARB sono stati usati più frequentemente in Asia. La prevalenza delle malattie cardiovascolari di base e del diabete era simile tra i partecipanti che utilizzavano ogni classe di farmaci antiipertensivi. Le caratteristiche di tutti i 46 studi inclusi sono disponibili nella eTabella 1 del supplemento.
Per tutti i 46 studi clinici inclusi nell’analisi, le variazioni medie (SD) della pressione sanguigna sistolica e diastolica complessive tra quelle riportate sono state rispettivamente di -18,0 (8,7) mm Hg e -10,1 (4,7) mm Hg. Il rischio complessivo di eventi cardiovascolari è stato dell’11,5%. Tra i profili degli effetti avversi, l’edema era prevalente tra lo 0,5% dei partecipanti che ricevevano ACE inibitori, il 17,1% dei partecipanti che ricevevano DH CCB o non-DH CCB, l’8,7% dei partecipanti che ricevevano β-bloccanti, il 15,1% dei partecipanti che ricevevano ARB, il 9,9% dei partecipanti che ricevevano diuretici, e il 3,7% dei partecipanti che ricevevano placebo. La tosse era prevalente tra l’8,3% dei partecipanti che ricevevano ACE inibitori, il 9,6% dei partecipanti che ricevevano DH CCB o non-DH CCB, il 4,1% dei partecipanti che ricevevano β-bloccanti, il 2,7% dei partecipanti che ricevevano ARB, il 5,4% dei partecipanti che ricevevano diuretici, e il 16,1% dei partecipanti che ricevevano placebo. Cefalea o ipotensione era prevalente tra lo 0,7% dei partecipanti che ricevevano ACE inibitori, il 7,9% dei partecipanti che ricevevano DH CCB o non-DH CCB, l’1,4% dei partecipanti che ricevevano β-bloccanti, il 10,8% dei partecipanti che ricevevano ARB, il 7,4% dei partecipanti che ricevevano diuretici, e l’8,8% dei partecipanti che ricevevano placebo. Le vertigini erano prevalenti tra l’1,7% dei partecipanti che ricevevano ACE inibitori, il 7,5% dei partecipanti che ricevevano DH CCB o non-DH CCB, il 9,1% dei partecipanti che ricevevano β-bloccanti, il 14,8% dei partecipanti che ricevevano ARB, il 9,0% dei partecipanti che ricevevano diuretici, e il 10,2% dei partecipanti che ricevevano placebo.

Figura 1.Diagramma PRISMA di ricerca e selezione della letteraturaI motivi di esclusione non sono stati categorizzati per singolo articolo perché ogni articolo può aver soddisfatto più criteri di esclusione.

Figura 2.Schema di rete dei farmaci antiipertensivi ACEi indica l’inibitore dell’enzima di conversione dell’angiotensina; ARB, bloccante del recettore dell’angiotensina; BB, β-bloccante; DH CCB, calcioantagonista diidropiridina; e non-DH CCB, calcioantagonista nondiidropiridina.
Efficacia comparativa
Una valutazione delle differenze di rischio assoluto degli eventi cardiovascolari tra gli studi clinici con placebo che hanno confrontato i farmaci antipertensivi con il placebo ha indicato che tutti e 5 i tipi di farmaci antipertensivi sono stati associati a una maggiore diminuzione degli eventi cardiovascolari rispetto al placebo. Rispetto al placebo, i DH CCB sono stati riportati per ridurre il rischio di morte cardiovascolare di 7 casi ogni 1000 persone; gli ACE inibitori e i diuretici sono stati riportati per ridurre il rischio di infarto del miocardio rispettivamente di 24 casi e 10 casi ogni 1000 persone; e i DH CCB e i diuretici sono stati riportati per ridurre il rischio di ictus rispettivamente di 16 casi e 21 casi ogni 1000 persone (eTabella 2 nel supplemento).
Sulla base di questi risultati, 143 persone avrebbero bisogno di essere trattate con DH CCB per prevenire 1 morte cardiovascolare. Per prevenire 1 infarto del miocardio, 42 persone dovrebbero essere trattate con ACE inibitori e 100 persone con diuretici. Per prevenire 1 ictus, 63 persone dovrebbero essere trattate con DH CCB e 48 persone con diuretici.
Meta-analisi di rete
Nella meta-analisi di rete che confronta il placebo con i gruppi di farmaci, per la morte cardiovascolare, abbiamo notato che gli ACE inibitori, i DH CCB, gli ARB e i diuretici erano tutti associati con una riduzione del rischio relativo del 15- 22%. Le riduzioni specifiche del rischio relativo erano le seguenti: per gli ACE inibitori, riduzione del 20% (95% IC, 9%-30%; RR, 0,80; 95% CI, 0,70-0,91); per i DH CCB, riduzione del 20% (95% CI, 11%-29%; RR, 0.80; 95% CI, 0,71-0,89); per gli ARB, riduzione del 15% (95% CI, 3%-26%; RR, 0,85; 95% CI, 0,74-0,97); e per i diuretici, riduzione del 22% (95% CI, 12%-31%; RR, 0,78; 95% CI, 0,69-0,88).
Per l’infarto del miocardio, gli ACE inibitori, gli ACE inibitori, i DH CCB e i β-bloccanti sono stati associati a riduzioni del rischio relativo dal 20% al 28%. Le riduzioni specifiche del rischio relativo sono state le seguenti: per gli ACE inibitori, riduzione del 28% (95% IC, 12%-41%; RR, 0,72; 95% CI, 0,59-0,88); per i DH CCB, riduzione del 21% (95% CI, 4%-34%; RR, 0,79; 95% CI, 0,66-0,96); e per i β-bloccanti, riduzione del 20% (95% CI, 1%-35%; RR, 0,80; 95% CI, 0,65-0,99).
Per l’ictus, tutte le classi di farmaci sono state associate a riduzioni del rischio relativo dal 19% al 39%. Le riduzioni specifiche del rischio relativo sono state le seguenti: per gli ACE inibitori, riduzione del 34% (95% IC, 20%-45%; RR, 0,66; 95% CI, 0,55-0,80); per i DH CCB, riduzione del 39% (95% CI, 30%-48%; RR, 0,61; 95% CI, 0,52-0.70); per i β-bloccanti, riduzione del 20% (95% IC, 2%-33%; RR, 0,80; 95% CI, 0,67-0,98); per gli ARB, riduzione del 31% (95% CI, 17%-42%; RR, 0,69; 95% CI, 0,58-0,83); e per i diuretici, riduzione del 37% (95% CI, 24%-47%; RR, 0,63; 95% CI, 0,53-0,76).
Per la rivascolarizzazione, i diuretici sono stati associati ad una riduzione del rischio relativo del 33% (95% CI, 5%-53%; RR, 0,67; 95% CI, 0,47-0,95). Per gli eventi cardiovascolari complessivi, tutte le classi di farmaci sono state associate a una riduzione del rischio relativo dal 17% al 29% (Figura 3). Le riduzioni specifiche del rischio relativo sono state le seguenti: per gli ACE inibitori, riduzione del 29% (95% IC, 17%-40%; RR, 0,71; 95% CI, 0,60-0,83); per i DH CCB, riduzione del 27% (95% CI, 16%-36%; RR, 0,73; 95% CI, 0,64-0.84); per i β-bloccanti, riduzione del 17% (95% IC, 2%-30%; RR, 0,83; 95% CI, 0,70-0,98); per gli ARB, riduzione del 21% (95% CI, 6%-33%; RR, 0,79; 95% CI, 0,67-0,94); e per i diuretici, riduzione del 27% (95% CI, 15%-38%; RR, 0,73; 95% CI, 0,62-0,85).
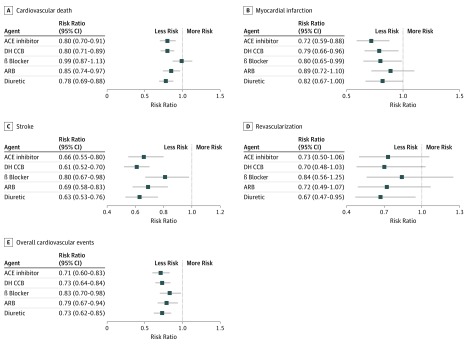
Figura 3.Figura 3. Meta-analisi di rete che confronta la singola classe di farmaci antiipertensivi con il placebo per il trattamento di eventi cardiovascolariACE indica l’enzima di conversione dell’angiotensina; ARB, bloccante del recettore dell’angiotensina; DH CCB, calcio-antagonista diidropiridina; e barre di errore, 95% CI.
Questi dati indicano che, a seconda delle dimensioni dell’effetto, gli ACE inibitori, i DH CCB e i diuretici erano associati a riduzioni altrettanto significative del rischio di eventi cardiovascolari complessivi e di morte cardiovascolare. Le maggiori riduzioni del rischio di infarto del miocardio sono state associate agli ACE inibitori, mentre i DH CCB e i diuretici sono stati associati a riduzioni altrettanto significative del rischio di ictus. I diuretici sono stati associati a riduzioni altrettanto significative del rischio di rivascolarizzazione. Tuttavia, i loro IC al 95% si sono sovrapposti.

Figura 3.Meta-analisi di rete che confronta la singola classe di farmaci antiipertensivi con il placebo per il trattamento di eventi cardiovascolariACE indica l’enzima di conversione dell’angiotensina; ARB, bloccante del recettore dell’angiotensina; DH CCB, calcio-antagonista diidropiridina; e barre di errore, 95% CI.
Coerenza, eterogeneità, polarizzazione e sensibilità
In termini di rischio di valutazione del bias, abbiamo trovato che gli studi erano di qualità moderata (punteggio medio, 4.0 di 5.0 punti possibili), in cui la randomizzazione aveva un punteggio medio (SD) di 1.8 (1.0) di 2.0 punti, la cecità aveva un punteggio medio (SD) di 1.1 (0.5) di 2.0 punti, e la considerazione di tutti i pazienti aveva un punteggio medio (SD) di 1.0 (1.0) di 1.0 punti. Nessuno studio è stato considerato ad alto rischio di distorsione. L’esame visivo dei diagrammi ad imbuto ha indicato che non era presente alcun pregiudizio significativo per la morte cardiovascolare, l’infarto del miocardio, l’ictus, la rivascolarizzazione e gli eventi cardiovascolari in generale (eFigure 1 nel supplemento).
Non è stata riscontrata alcuna incongruenza generale dell’effetto del trattamento su ciascun risultato, con tutti i valori di P superiori a .05. Con il trattamento individuale, non è stata rilevata alcuna incongruenza significativa tra le diverse classi di farmaci antiipertensivi (eTabella 3 nel supplemento). Non è stata rilevata alcuna eterogeneità significativa dell’effetto del trattamento, in quanto nessuno dei valori τ 2 era uguale o superiore a 0,25 (eTabella 2 nel supplemento).
In metaregressioni di riduzione della pressione sanguigna con eventi cardiovascolari, la riduzione della pressione sanguigna è stata associata a riduzioni di eventi cardiovascolari. In particolare, ogni riduzione di 10 mm Hg di pressione sanguigna sistolica è stata significativamente associata a un rischio di morte cardiovascolare inferiore del 13% (RR, 0,87; 95% IC, 0,77-0,99), un rischio di ictus inferiore del 17% (RR, 0,83; 95% CI, 0,72-0,97) e un rischio di eventi cardiovascolari complessivi inferiore del 14% (RR, 0,86; 95% CI, 0,78-0,96). Ogni riduzione di 5 mm Hg di pressione diastolica è stata significativamente associata a un rischio di morte cardiovascolare inferiore del 14% (RR, 0,86; 95% CI, 0,74-1,00), un rischio di ictus inferiore del 20% (RR, 0,80; 95% CI, 0,67-0,95) e un rischio inferiore del 16% di eventi cardiovascolari complessivi (RR, 0,84; 95% CI, 0,74-0,96; eTabella 4 nel supplemento).
Discussione
Da 46 studi clinici randomizzati che hanno esaminato l’effetto dei farmaci antiipertensivi più comunemente usati sulla prevenzione degli eventi cardiovascolari, i risultati congiunti hanno mostrato che gli ACE inibitori, i DH CCB e i diuretici sono risultati altrettanto efficaci nella prevenzione della morte cardiovascolare (circa il 20% di riduzione rispetto al placebo), dell’ictus (circa il 35% di riduzione rispetto al placebo) e degli eventi cardiovascolari complessivi (circa il 30% di riduzione rispetto al placebo). Gli inibitori dell’enzima di conversione dell’angiotensina sono stati indicati come i più efficaci nella prevenzione dell’infarto del miocardio (circa 30% di riduzione rispetto al placebo). I diuretici sono stati indicati come i più efficaci nel ridurre la rivascolarizzazione (circa il 30% rispetto al placebo). Il nostro studio fornisce le prove più attuali ad oggi sull’efficacia comparativa dei farmaci antiipertensivi segnalati per ridurre gli eventi cardiovascolari in studi clinici randomizzati. Inoltre, a nostra conoscenza, questa è la prima meta-analisi a mettere insieme i risultati di studi che hanno testato l’efficacia dei farmaci antiipertensivi nel ridurre il rischio di rivascolarizzazione.
I nostri risultati sono coerenti con quelli riportati nelle precedenti meta-analisi di studi clinici randomizzati.8,9 Psaty et al9 ha trovato che i diuretici a basso dosaggio sono stati segnalati come il trattamento più efficace per prevenire il verificarsi di mortalità cardiovascolare. Legge e altri8 ha indicato che per l’ictus, tutte le classi di farmaci antiipertensivi sono stati segnalati per avere effetti simili di riduzione del rischio per una data riduzione della pressione sanguigna. I nostri risultati hanno ulteriormente supportato le prove che indicano che le differenze segnalate degli effetti sulla riduzione degli eventi cardiovascolari tra le classi di farmaci sono piccole. Abbiamo anche fornito informazioni più aggiornate sull’efficacia dei farmaci antipertensivi nella riduzione degli eventi cardiovascolari. Una recente analisi sistematica multinazionale, lo studio LEGEND-HTN (Large-Scale Evidence Generation and Evaluation Across a Network of Databases for Hypertension),21 ha usato dati osservazionali che comprendono milioni di pazienti e ha scoperto che i diuretici sono stati associati a vantaggi nella riduzione di vari eventi cardiovascolari rispetto ad altre classi di farmaci. Questo risultato è diverso da quello del nostro studio, che ha indicato che i diuretici avevano un’efficacia simile a quella riportata per la riduzione degli eventi cardiovascolari rispetto agli ACE inibitori e ai DH CCB e che gli ACE inibitori sembravano essere più efficaci nel ridurre l’infarto del miocardio. La differenza nei risultati può essere dovuta ai diversi disegni dello studio (studi clinici randomizzati vs. studi osservazionali), e non è chiaro in che misura lo studio LEGEND-HTN possa essere soggetto a distorsioni di selezione.
La meta-analisi della rete ci ha permesso di confrontare le classi di farmaci con il placebo sia direttamente (cioè, tra gli studi placebo-clinici inclusi) che indirettamente (cioè, tra tutti gli studi inclusi). I confronti tra farmaci e placebo hanno indicato lievi differenze tra i confronti diretti e quelli complessivi. I confronti in rete sono stati più precisi (cioè, avevano IC più ristretti del 95%).
Vale anche la pena di notare che l’associazione tra la diminuzione della pressione sanguigna e la riduzione degli eventi cardiovascolari era inferiore a quella ottenuta dagli studi osservazionali.22,23 Il motivo può essere che la maggior parte dei partecipanti agli studi clinici, compresi quelli che hanno ricevuto placebo, sono stati motivati a ridurre la loro pressione sanguigna e, in alcuni casi, sono stati trattati anche con altri farmaci. Inoltre, la motivazione dei partecipanti può averli portati ad adottare abitudini di vita sane, come scegliere modelli di dieta più sani, fare esercizio fisico ed evitare l’uso di tabacco e alcol. La modificazione della dieta può e deve essere uno sforzo complementare per cercare di ridurre la BP e molti modelli dietetici sono supportati da solide prove.27 Questa constatazione richiede anche studi futuri che esaminino le associazioni tra i farmaci antiipertensivi e lo stile di vita nella prevenzione degli eventi cardiovascolari tra i pazienti con ipertensione. Tuttavia, sebbene l’entità dell’effetto dell’associazione tra la diminuzione della pressione sanguigna e la riduzione degli eventi cardiovascolari fosse piccola, alcune delle differenze erano statisticamente significative.
Limitazioni
Il nostro studio è stato limitato dal numero relativamente piccolo di studi inclusi nella meta-analisi della rete, quindi ci mancava il potere statistico di condurre analisi di sottogruppo per esaminare se l’associazione dei farmaci antiipertensivi con eventi cardiovascolari ridotti potesse essere la conseguenza di diversi fattori (ad esempio, età, sesso o livello di pressione sanguigna di base). Sebbene i risultati di questa analisi possano servire come fonte di riferimento, è necessario uno studio completo basato su fattori demografici e comorbidità per valutare quale classe di farmaci antipertensione dovrebbe essere raccomandata per ridurre gli esiti cardiovascolari avversi. Le linee guida per l’ipertensione pubblicate di recente dall’American College of Cardiology e dall’American Heart Association identificano una gamma più ampia di individui con ipertensione e preipertensione precoci, e il nostro studio può guidare le scelte dei farmaci di prima linea.24 Inoltre, i 46 studi clinici che abbiamo studiato sono stati eseguiti per lo più in Nord America, Europa occidentale e Asia orientale, e sono necessari ulteriori dati sui pazienti dell’Asia meridionale e dell’Africa, che cumulativamente costituiscono un’ampia percentuale della popolazione mondiale.
Un altro importante limite del nostro studio è che non abbiamo incluso i risultati per le combinazioni di farmaci antiipertensivi perché c’erano troppo pochi studi con dati per ogni permutazione di combinazioni. Tuttavia, questa mancanza di studi suggerisce che l’efficacia di diversi gruppi di combinazioni, come i β-bloccanti e i diuretici, dovrà essere studiata più frequentemente in futuro. Recenti risultati hanno indicato che il trattamento con basse dosi di 3 farmaci antipertensivi è associato a una maggiore percentuale di pazienti che hanno raggiunto la pressione sanguigna target rispetto alle cure standard,25 e le terapie a quarti di dose con farmaci combinati sono risultate più efficaci, con meno eventi avversi, nel ridurre la pressione sanguigna rispetto alla monoterapia standard.26
Conclusioni
L’attuale meta-analisi della rete ha indicato che i principali farmaci antiipertensivi di prima linea, tra cui ACE inibitori, DH CCB, β-bloccanti, ARB e diuretici, sono risultati tutti efficaci nel ridurre gli eventi cardiovascolari rispetto al placebo. Inoltre, gli ACE inibitori, i DH CCB e i diuretici sono risultati altrettanto efficaci nel ridurre i decessi cardiovascolari, l’ictus e gli eventi cardiovascolari in generale. Rispetto ad altri farmaci antiipertensivi, gli ACE inibitori sono sembrati essere i farmaci di scelta per prevenire l’infarto del miocardio e i diuretici sono sembrati essere la scelta ottimale per ridurre la rivascolarizzazione. Le differenze tra le classi di farmaci erano generalmente piccole in termini di associazioni con la riduzione degli eventi cardiovascolari. Gli studi futuri dovrebbero confrontare l’efficacia di più farmaci antiipertensivi in combinazione con i singoli farmaci antiipertensivi nella riduzione degli eventi cardiovascolari.
References
- Global, regional, and national comparative risk assessment of 79 behavioural, environmental and occupational, and metabolic risks or clusters of risks in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet. 2015; 386(10010)DOI | PubMed
- Publisher Full Text
- Hypertension and cardiovascular disease: contributions of the Framingham heart study. Glob Heart. 2013; 8(1):49-57. DOI | PubMed
- Worldwide prevalence of hypertension exceeds 1.3 billion. J Am Soc Hypertens. 2016; 10(10):753-754. DOI | PubMed
- Impact of 2017 ACC/AHA guidelines on prevalence of hypertension and eligibility for antihypertensive treatment in United States and China: nationally representative cross sectional study. BMJ. 2018; 362:k2357. DOI | PubMed
- Implications of the New American College of Cardiology guidelines for hypertension prevalence in India. JAMA Intern Med. 2018; 178(10):1416-1418. DOI | PubMed
- Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet. 2016; 387(10022):957-967. DOI | PubMed
- Use of blood pressure lowering drugs in the prevention of cardiovascular disease: meta-analysis of 147 randomised trials in the context of expectations from prospective epidemiological studies. BMJ. 2009; 338:b1665. DOI | PubMed
- Health outcomes associated with various antihypertensive therapies used as first-line agents: a network meta-analysis. JAMA. 2003; 289(19):2534-2544. DOI | PubMed
- 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ASPC/NMA/PCNA guideline for the prevention, detection, evaluation, and management of high blood pressure in adults: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Hypertension. 2018; 71(6):1269-1324. DOI | PubMed
- Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. BMJ. 2009; 339:b2535. DOI | PubMed
- Assessing the quality of reports of randomized clinical trials: is blinding necessary?. Control Clin Trials. 1996; 17(1):1-12. DOI | PubMed
- Ranking treatments in frequentist network meta-analysis works without resampling methods. BMC Med Res Methodol. 2015; 15:58. DOI | PubMed
- Graphical tools for network meta-analysis in STATA. PLoS One. 2013; 8(10)DOI | PubMed
- Extending DerSimonian and Laird’s methodology to perform network meta-analyses with random inconsistency effects. Stat Med. 2016; 35(6):819-839. DOI | PubMed
- Two new methods to fit models for network meta-analysis with random inconsistency effects. BMC Med Res Methodol. 2016; 16:87. DOI | PubMed
- Consistency and inconsistency in network meta-analysis: concepts and models for multi-arm studies. Res Synth Methods. 2012; 3(2):98-110. DOI | PubMed
- Network meta-analysis: application and practice using Stata. Epidemiol Health. 2017; 39DOI | PubMed
- Meta-analyses: how to read a funnel plot. BMJ. 2013; 346:f1342. DOI
- Meta-regression in Stata. Stata J. 2008; 8(4):493-519. DOI
- Comprehensive comparative effectiveness and safety of first-line antihypertensive drug classes: a systematic, multinational, large-scale analysis. Lancet. 2019; 394(10211):1816-1826. DOI | PubMed
- Blood pressure, stroke, and coronary heart disease: part 1, prolonged differences in blood pressure: prospective observational studies corrected for the regression dilution bias. Lancet. 1990; 335(8692):765-774. DOI | PubMed
- Blood pressure and cardiovascular disease in the Asia Pacific region. J Hypertens. 2003; 21(4):707-716. DOI | PubMed
- Prevention, detection, evaluation, and management of high blood pressure in adults: synopsis of the 2017 American College of Cardiology/American Heart Association hypertension guideline. Ann Intern Med. 2018; 168(5):351-358. DOI | PubMed
- Fixed low-dose triple combination antihypertensive medication vs usual care for blood pressure control in patients with mild to moderate hypertension in Sri Lanka: a randomized clinical trial. JAMA. 2018; 320(6):566-579. DOI | PubMed
- Efficacy and safety of quarter-dose blood pressure–lowering agents: a systematic review and meta-analysis of randomized controlled trials. Hypertension. 2017; 70(1):85-93. DOI | PubMed
- Effects of different dietary interventions on blood pressure: systematic review and meta-analysis of randomized controlled trials. Hypertension. 2016; 67(4):733-739. DOI | PubMed
Fonte
Wei J, Galaviz KI, Kowalski AJ, Magee MJ, Haw JS, et al. (2020) Comparison of Cardiovascular Events Among Users of Different Classes of Antihypertension Medications. JAMA Network Open 3(2): e1921618. https://doi.org/10.1001/jamanetworkopen.2019.21618





