Abstract
Punti di sintesi
- Molti interventi sanitari ritenuti convenienti in termini di costi non sono accessibili. Nonostante l’importanza dell’accessibilità economica per i responsabili politici, poca della letteratura sul rapporto costo-efficacia nella sanità globale affronta questo problema.
- L’analisi dell’impatto del budget (BIA) descrive i costi e i risparmi a breve termine di un intervento dal punto di vista del pagatore.
- I ricercatori dovrebbero riportare la BIA insieme all’analisi costo-efficacia (CEA). Quando CEA e BIA portano a conclusioni diverse, i ricercatori dovrebbero spiegare perché.
- I decisori politici dovrebbero riconoscere che non tutti gli interventi economicamente convenienti sono accessibili e interpretare le informazioni sul rapporto costo-efficacia nel contesto del loro budget e delle altre fonti di finanziamento disponibili.
- Sia il rapporto costo-efficacia che l’accessibilità economica dovrebbero riflettersi nella progettazione di pacchetti di servizi sanitari essenziali.
Introduzione
Gli Obiettivi di Sviluppo Sostenibile post 2015 invitano i governi a combattere le malattie infettive, a ridurre la mortalità materna e infantile e a garantire che l’assistenza sanitaria di qualità sia accessibile e alla portata di tutti[1]. Per raggiungere questi obiettivi, circa la metà dei Paesi sta compiendo sforzi per introdurre o estendere la copertura sanitaria universale (UHC)[2]. Questo processo richiede che i governi definiscano pacchetti di servizi essenziali garantiti a tutti i cittadini. A causa delle limitazioni delle risorse, questi pacchetti non possono includere tutti i servizi sanitari. Di conseguenza, sia i ricercatori che i responsabili politici hanno raccomandato di dare priorità agli interventi economicamente convenienti[3-5].
Tuttavia, gli interventi economicamente convenienti non sono sempre accessibili. In alcuni casi, l’adozione di interventi efficaci dal punto di vista dei costi richiederebbe l’eliminazione di altre spese più vantaggiose. In un esempio molto pubblicizzato, i nuovi farmaci per l’epatite cronica C sono stati trovati convenienti in molti contesti, anche a prezzi elevati[6- 8], ma la fornitura di questi farmaci a tutti i potenziali beneficiari è stata inaccessibile, anche con sconti [9,10]. Le sfide di accessibilità economica sono sorte anche con numerosi altri interventi, tra cui i vaccini per il papillomavirus umano (HPV) e le infezioni da pneumococco[11,12] e la diagnostica della tubercolosi GeneXpert[13,14]. Questo scollamento tra costo-efficacia e accessibilità economica può complicare gli sforzi per identificare e adottare programmi di alto valore.
Questo documento valuta innanzitutto l’uso attuale dell’analisi dell’impatto del bilancio (BIA) e dell’analisi del rapporto costo-efficacia (CEA) nelle valutazioni economiche sulla salute condotte per i paesi a basso e medio reddito (LMIC) (Tabella 1). Raccomandiamo quindi ai ricercatori e ai responsabili delle politiche di integrare meglio le informazioni sull’accessibilità economica nelle valutazioni economiche della salute, insieme al CEA.
| CEA | BIA | |
|---|---|---|
| Obiettivo | Quantificare il rendimento netto dell’investimento per la salute di un intervento | Quantificare l’impatto di un intervento sulle risorse consumate |
| Risultati | Benefici netti per la salute, consumo netto di risorse | Consumo netto di risorse |
| Prospettiva | Societario, settore sanitario o pagante | Pagatore |
| Orizzonte temporale | A lungo termine (fino alla realizzazione di tutti i costi e i benefici) | Ciclo di bilancio (tipicamente 1-5 anni) |
| Unità | ICER=Costsintervention-CostscomparatorBenefitsintervention-Benefitscomparator | Costi e risparmi assoluti ($) |
| Interpretazione | Un ICER più piccolo indica minori costi per unità di salute guadagnata, cioè una maggiore efficienza dei costi | I costi più bassi indicano una maggiore accessibilità economica |
| Soglia | Un nuovo intervento è “conveniente” se ICER scende al di sotto di una soglia WTP | Non c’è uno standard per valutare l’accessibilità economica di ogni singolo intervento |
Stato attuale di CEA e BIA
Mentre i fattori politici, sociali e culturali giocano un ruolo importante nell’allocazione del budget, il CEA può informare le decisioni su come massimizzare i rendimenti sanitari con risorse limitate. Nell’ultimo decennio è aumentato anche l’interesse per la valutazione dell’accessibilità economica[9,15,16]. La BIA valuta l’accessibilità economica stimando i costi netti a breve termine di un intervento dal punto di vista del pagatore [17]. Molti paesi, tra cui il Canada, il Regno Unito, il Brasile e la Tailandia, richiedono sia la BIA che la CEA nel valutare se includere un farmaco in un formulario pubblico[17-20]. Nel 2014, la Bill & Melinda Gates Foundation ha anche raccomandato di includere sia la BIA che la CEA nelle valutazioni economiche sulla salute [21]. Tuttavia, la BIA è raramente considerata nei quadri di definizione delle priorità per l’UHC[16].
Inoltre, la letteratura economica sulla salute valutata tra pari per le LMIC spesso manca di informazioni sull’impatto del bilancio. Per esempio, abbiamo studiato l’uso della BIA negli articoli catalogati nel registro del Tufts Medical Center Global Health Cost-Effectiveness Analysis (GHCEA). Il Registro GHCEA contiene informazioni su tutti gli articoli CEA in lingua inglese sottoposti a peer-reviewing con benefici per la salute misurati in termini di anni di vita mediati (DALYs)[22]. Abbiamo scoperto che solo il 3%(n/N= 12/384) degli articoli del GHCEA ha condotto una BIA formale, menzionando esplicitamente la BIA nelle sezioni metodi e risultati. Un altro 10% degli articoli(n/N = 37/384) includeva informalmente qualche misura di impatto sul budget, spesso nella sezione di discussione. (Vedi S1 Testo per i criteri di inclusione e S1 Tabella per gli articoli inclusi).
Quando gli articoli presentavano sia il CEA che la BIA, le loro raccomandazioni spesso divergevano. Più della metà degli articoli che riportavano i risultati formali o informali della BIA concludeva che gli interventi economicamente convenienti potevano essere inaccessibili (Fig. 1). Uno ha dichiarato: “Le realtà finanziarie che i sistemi sanitari dei Paesi in via di sviluppo, privi di risorse, rendono impossibile realizzare tutti gli interventi potenzialmente “molto efficaci in termini di costi” [23]. Altri hanno concluso che i budget dei programmi[24] o anche i budget sanitari nazionali[25] avrebbero dovuto essere triplicati o quadruplicati per poter accogliere interventi efficaci dal punto di vista dei costi.
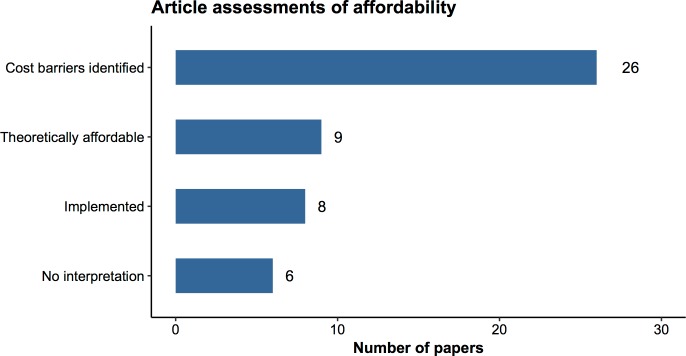
Fig. 1.Valutazioni dell’accessibilità economica nella letteratura sul rapporto costo/efficacia.Le categorie riflettono le valutazioni dell’autore sull’accessibilità economica basate sui risultati della BIA. Le “barriere di costo identificate” indicano che l’autore ha identificato uno o più fattori che potrebbero rendere un intervento non accessibile. Gli interventi “teoricamente accessibili” sono stati ritenuti fattibili con le risorse attuali e/o con il supporto esterno disponibile (ad es, Gli interventi “implementati” erano già stati implementati al momento della pubblicazione. “Nessuna interpretazione” indica che l’autore ha condotto una BIA ma non ha fatto dichiarazioni sull’accessibilità economica dell’intervento. Esempi di come abbiamo classificato le valutazioni appaiono nel testo S2. Fonte dei dati: estrazione dell’autore dal registro GHCEA(www.ghcearegistry.org). Abbreviazioni: BIA, analisi dell’impatto del budget; GHCEA, Global Health Cost-Effectiveness Analysis.
Alcuni articoli suggeriscono riduzioni di prezzo per affrontare i problemi di accessibilità economica[12,26,27]. Uno ha scritto: “si spera che [il prezzo del vaccino contro il rotavirus] venga ridotto alla luce di questa analisi” [28], e un altro ha raccomandato una politica di negoziazione dei farmaci più forte per i vaccini contro il colera [23]. Altri hanno suggerito che risorse aggiuntive da parte di finanziatori esterni potrebbero sovvenzionare i costi del programma[12,26,29]. Per esempio, per un programma di gestione della malaria a domicilio, un articolo affermava che “i costi di allestimento possono essere particolarmente adatti per il finanziamento da parte delle organizzazioni donatrici… mentre i costi successivi potrebbero essere contenuti nel budget di un tipico Distretto dell’Africa subsahariana” [30].

Fig. 1.Fig. 1. Valutazioni dell’accessibilità economica nella letteratura sul rapporto costo-efficacia.Le categorie riflettono le valutazioni dell’autore sull’accessibilità economica basate sui risultati della BIA. Le “barriere di costo identificate” indicano che l’autore ha identificato uno o più fattori che potrebbero rendere un intervento non accessibile. Gli interventi “teoricamente accessibili” sono stati ritenuti fattibili con le risorse attuali e/o con il supporto esterno disponibile (ad es, Gli interventi “implementati” erano già stati implementati al momento della pubblicazione. “Nessuna interpretazione” indica che l’autore ha condotto una BIA ma non ha fatto dichiarazioni sull’accessibilità economica dell’intervento. Esempi di come abbiamo classificato le valutazioni appaiono nel testo S2. Fonte dei dati: estrazione dell’autore dal registro GHCEA(www.ghcearegistry.org). Abbreviazioni: BIA, analisi dell’impatto del budget; GHCEA, Global Health Cost-Effectiveness Analysis.
Prossimi passi avanti: Conciliare costo-efficacia e accessibilità economica
Come possono essere economicamente convenienti gli interventi?
Il divario tra il rapporto costo-efficacia e l’accessibilità economica può confondere perché il CEA sembra rendere conto dell’accessibilità economica: esso confronta il valore di un intervento con una misura di volontà sociale di pagare (WTP) per i miglioramenti della salute (Tabella 1). Tuttavia, il CEA affronta la questione dell’accessibilità economica solo indirettamente e in modo incompleto.
In teoria, CEA parte dal presupposto che un policymaker condurrebbe una “shopping spree” con un budget fisso e informazioni sul rapporto costo-efficacia di tutti i programmi disponibili. Al fine di decidere quali programmi finanziare, il policymaker avrebbe dovuto classificare i programmi in primo luogo in base al rapporto costo-efficacia incrementale (ICER) (Tabella 1), una misura del rapporto costo-efficacia. Il policymaker adotterebbe poi programmi in ordine di efficacia dei costi, continuando fino all’esaurimento del budget sanitario. Poiché la “shopping spree” continua solo fino all’esaurimento del budget, l’insieme dei programmi selezionati è, per definizione, conveniente. L’ICER dell’ultimo programma adottato (cioè il programma meno conveniente del budget) è designato come soglia WTP. I programmi con ICER inferiori alla soglia sono sia economici che abbordabili.
In pratica, tuttavia, gli articoli della CEA in genere considerano solo pochi interventi e non conducono una “shopping spree”, ma la soglia di costo-efficacia è identificata in modo esogeno. I ricercatori misurano il costo aggregato della morte e della disabilità in anni di vita corretti per la disabilità (DALYs) o anni di vita corretti per la qualità (QALYs), che riflettono entrambi la longevità e la qualità della vita. Guadagnare un anno di vita in perfetta salute, per esempio, evita 1 DALY, mentre guadagnando un anno di vita in uno stato di salute meno favorito si evita una frazione di un DALY, a seconda della gravità della morbilità per quello stato di salute. La letteratura sull’economia della salute spesso definisce gli interventi che evitano un DALY (o guadagnano un QALY) per non più di 1-3 volte il prodotto interno lordo (PIL) pro capite di un paese come “conveniente”, il che è giustificato dall’affermazione che un paese dovrebbe essere disposto a pagare per un anno di vita circa quanto una persona media produrrebbe in quell’anno. In molti Paesi, tuttavia, i bilanci sanitari non sono abbastanza grandi per finanziare tutti gli interventi con ICER al di sotto di questo tetto[31]. Pertanto, alcuni interventi economicamente convenienti non sono accessibili.
Spiegare la divergenza tra accessibilità economica e rapporto costo-efficacia
Dimensioni del budget e soglia WTP
Uno dei motivi per cui BIA e CEA possono divergere è che la soglia di WTP presunta in CEA è troppo alta. Supponiamo che il budget di un paese non sia sufficiente a sostenere tutti i programmi con ICER al di sotto della soglia WTP. Se il budget sanitario riflette le preferenze della popolazione per quanto riguarda il livello adeguato di spesa per la salute (o altrimenti non può essere aumentato), allora la vera soglia WTP deve essere inferiore a quella ipotizzata. Idealmente, la soglia del WTP dovrebbe riflettere la spesa corrente, e i ricercatori hanno iniziato a stimare le soglie empiriche sulla base del bilancio corrente di un paese [31].
Tuttavia, la revisione della soglia del WTP presenta diverse sfide. Le soglie empiriche sono difficili da calcolare perché il processo richiede la conoscenza del rapporto costo-efficacia di tutti i programmi finanziati. Inoltre, è comune che alcuni programmi non finanziati siano più convenienti in termini di costi rispetto a quelli finanziati. Anche se il budget sanitario è teoricamente abbastanza grande da finanziare tutti gli interventi economicamente convenienti, se una parte di quel budget viene dirottata per finanziare interventi che non sono convenienti, allora alcuni interventi economicamente convenienti potrebbero non essere convenienti. In sistemi sanitari complessi e in rapida evoluzione, il CEA non può fornire regole semplici. Anche programmi “economicamente convenienti” di alto valore possono richiedere più risorse di quelle disponibili in un determinato budget.
Pochi LMIC attualmente soddisfano gli obiettivi di spesa dell’OMS per la spesa sanitaria pro capite[32], e diversi studi nel nostro campione hanno sottolineato la necessità di aumentare i budget sanitari complessivi[25,33]. In alcuni casi, l’evidenza del rapporto costo-efficacia può aumentare la volontà politica di dedicare risorse ai servizi sanitari di alto valore. Tuttavia, forti aumenti di budget potrebbero non essere politicamente o economicamente fattibili a causa delle risorse limitate. Riconoscendo questo, alcuni documenti raccomandano di iniziare con interventi di valore più elevato e a basso costo. Per esempio, un articolo suggeriva di espandere i programmi di screening non radiologico, molto convenienti dal punto di vista economico, per il cancro al seno in Messico e in Costa Rica, se non fosse possibile stanziare nuove risorse sostanziali per la mammografia, o per concentrare la mammografia sui gruppi a più alto rischio[24].
Prospettiva analitica
Alcuni autori attribuiscono la divergenza dell’accessibilità economica e del rapporto costo-efficacia principalmente alle differenze nel modo in cui questi due approcci stimano i valori del WTP[34]. Tuttavia, questa visione minimizza altre differenze tra i due tipi di analisi. Ad esempio, i CEA spesso adottano una prospettiva sociale, che include i costi sostenuti dai pazienti[35], o una prospettiva sanitaria, che include i pagamenti da parte di terzi. Al contrario, la BIA include solo i costi del pagatore. La scelta della prospettiva può influenzare fortemente le stime dell’ICER e può evidenziare casi in cui un programma allevia o esacerba un grande onere finanziario per i pazienti o altri segmenti della società. Per esempio, un’analisi della vaccinazione contro il rotavirus ha mostrato che incorporando i costi finanziari e di produttività sostenuti dai pazienti, l’ICER è diminuito del 30%-75% [36]. Un altro articolo ha rilevato che, se le stime dei costi sono state ridotte dall’entità dei sussidi forniti da Gavi, la vaccinazione contro il rotavirus ICER è diminuita del 50%[29].
Distribuzione dei costi e dei benefici
La maggior parte delle linee guida per la conduzione del CEA suggerisce che i rapporti costo-efficacia dovrebbero essere confrontati con una soglia WTP per valutare il rapporto qualità/prezzo. Se un nuovo intervento ha un ICER inferiore (cioè più favorevole) alla soglia, è teoricamente possibile adottare questa alternativa al posto di un programma esistente meno efficiente. In pratica, questa sostituzione potrebbe non essere fattibile perché i programmi con ICER più favorevoli possono anche fare richieste molto più grandi sul budget. Ad esempio, la sostituzione di un programma che costa 1 milione di dollari e che evita 50.000 DALY (20 dollari per DALY evitati) con un programma più efficiente che costa 10 milioni di dollari e che evita 1 milione di DALY (10 dollari per DALY evitati) aumenta la spesa sanitaria di 9 milioni di dollari. Trovare i 9 milioni di dollari in più potrebbe non essere possibile. Inoltre, alcuni programmi potrebbero non conferire pieni benefici per decenni. Il rapporto costo-efficacia incorpora le compensazioni dei costi, ma poiché tali compensazioni possono verificarsi in un lontano futuro, maturano per diversi programmi e pagatori e possono essere incerte, sono meno salienti per considerazioni di budget a breve termine.
Sia i costi elevati che le compensazioni dei costi ritardati sono stati salienti nella valutazione dei nuovi farmaci per il virus dell’epatite C (HCV), che sono convenienti in termini di costi, ma molto più costosi dei precedenti farmaci per l’HCV. Un’analisi ha stimato che il trattamento di tutti i pazienti con questi farmaci comporterebbe costi pari al 10% di tutte le spese farmaceutiche in diversi paesi[10,37]. Mentre i farmaci sono associati a compensazioni di costo, queste ultime non maturano per decenni. Di conseguenza, i Paesi che hanno adottato questi farmaci hanno spesso negoziato prezzi bassi, anche se i prezzi più alti erano convenienti (ad esempio, l’Egitto) o l’accesso limitato ai farmaci (ad esempio, gli Stati Uniti)[9,10,38,39].
Sconti
Un’ultima ragione per le incoerenze tra CEA e BIA deriva dalle differenze nel modo in cui trattano gli sconti. Il CEA sconta costi e benefici, tipicamente ad un tasso del 3% annuo[40,41]. Al contrario, le linee guida della BIA non raccomandano lo sconto perché il budget deve includere tutti i costi e perché spesso non è possibile investire un budget sanitario e ottenere un ritorno[17]. In generale, l’uso dell’attualizzazione rende più favorevoli i programmi con benefici che si verificano a breve termine e quelli con benefici ritardati (ad esempio, molti programmi di prevenzione) sembrano meno favorevoli.
Raccomandazioni
Per ovviare al fatto che gli interventi ritenuti economicamente convenienti nella letteratura pubblicata non sono sempre accessibili, proponiamo di includere informazioni sui costi di implementazione insieme all’efficacia dei costi. In primo luogo, i ricercatori dovrebbero presentare la BIA insieme al CEA. Per la maggior parte dei servizi sanitari non sono disponibili informazioni sull’impatto del bilancio. Se è possibile stimare la dimensione della popolazione ammissibile di un programma, la BIA standardizzata può essere facilmente condotta utilizzando le informazioni già sviluppate per il CEA (vedi Fig. 2). Come minimo, questo dovrebbe includere i costi e le compensazioni di costo su un orizzonte temporale breve; se possibile, i ricercatori dovrebbero confrontare i costi con il budget locale disponibile.
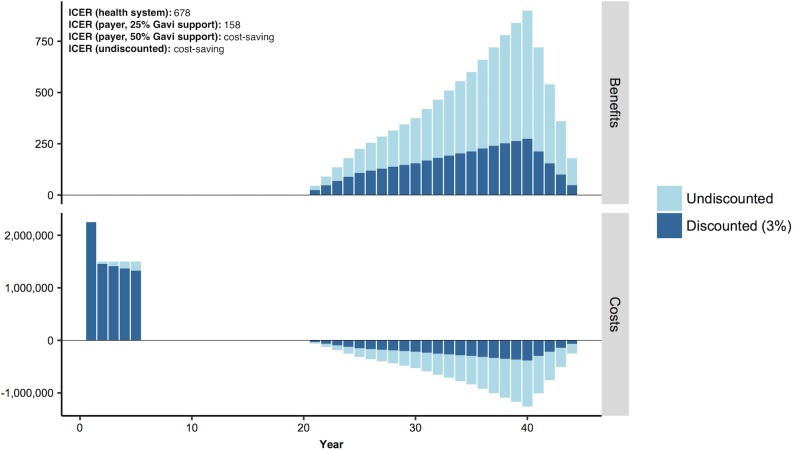
Fig. 2.Distribuzione dei costi e dei benefici all’anno per un intervento di vaccinazione stilizzato.L’altezza totale della barra è il costo o il beneficio non scontato. La parte blu scuro della barra è il valore attuale dei costi o benefici con un tasso di sconto annuale del 3%. Abbreviazione: ICER, rapporto costi/benefici incrementale.
In secondo luogo, i ricercatori dovrebbero evidenziare le possibili ragioni di divergenza tra CEA e BIA, che possono aiutare a identificare e dare priorità ai programmi di alto valore. Questi possono aiutare i decisori politici a interpretare le valutazioni del rapporto costo-efficacia alla luce delle risorse disponibili (1) identificando pacchetti di servizi ad alto rendimento condizionati dai budget esistenti e (2) suggerendo aree che produrrebbero alti benefici dall’aumento degli investimenti. In Tabella 2Riassumiamo queste raccomandazioni per la ricerca e la politica.
| Ricerca | Politica/pubblicità | ||
|---|---|---|---|
| Conduzione BIA | Aggiungi BIA a CEA | Richiesta CEA e BIA | |
| Costi e risparmi | Segnalare i costi e i risparmi non scontati per il pagatore su un orizzonte temporale di 1-5 anni nella valuta del paese corrente | Nella maggior parte dei casi, non tutti gli interventi “economici” rientrano nel budget. Confrontare il rapporto costo-efficacia relativo delle diverse strategie. A parità di altre condizioni, scegliere interventi con ICER inferiori. Puntare a ridurre la spesa per gli interventi con ICER alti, e aumentare la spesa per quelli con ICER bassi. | |
| Benchmark | Costo del benchmark in percentuale del budget attuale | ||
| Contesto | Indicare i programmi che potrebbero essere ridotti o eliminati per aggiungere nuovi interventi | ||
| Combinare BIA e CEA | Confronta CEA e BIA | Utilizzare la BIA per informare il CEA | |
| Orizzonte temporale | Segnalare i costi e i benefici maturati all’anno | Cercare un supporto esterno per programmi con ICER favorevoli ma con costi iniziali elevati. | |
| Prospettiva | Segnala il settore sanitario, la società e i contribuenti ICER | Identificare le opportunità di ripartizione dei costi tra i vari settori, in particolare quando i benefici sono condivisi tra i diversi settori. | |
| Sconti | Segnala gli ICER scontati e non scontati | Lavorare con i ricercatori per garantire che gli sconti riflettano le preferenze locali e le opportunità di investimento. |

Fig. 2.Fig. 2. Distribuzione dei costi e dei benefici all’anno per un intervento di vaccinazione stilizzato.L’altezza totale della barra è il costo o il beneficio non scontato. La parte blu scuro della barra è il valore attuale del costo o del beneficio con un tasso di sconto annuale del 3%. Abbreviazione: ICER, rapporto costi/benefici incrementale.
Esempio
Esploriamo un breve esempio di come queste raccomandazioni possano informare la ricerca e la politica (si veda il testo S3 per la derivazione). In Fig. 2Per un esempio stilizzato basato sulla vaccinazione contro l’HPV di 5 coorti, ognuna delle 100.000 ragazze di 10 anni in un paese a basso reddito, mostriamo costi e benefici all’anno[12,42- 44]. Mentre il sistema sanitario ICER sarebbe efficiente in termini di costi sulla base del PIL pro capite in molti Paesi, tutti i costi sono sostenuti in anticipo, mentre i benefici non sarebbero sperimentati per decenni. Stimiamo un costo di circa 8,25 milioni di dollari per un programma di vaccinazione quinquennale, con i costi più alti nel primo anno del programma. Pochi LMIC potrebbero sostenere questa spesa. Per esempio, nel 2015, le spese governative per le vaccinazioni di routine sono state in media di circa 9 milioni di dollari nei Paesi dell’Africa subsahariana[45]. Sulla base di questa media, e dei costi annuali per un nuovo vaccino nel nostro esempio, l’intervento aggiuntivo richiederebbe un aumento del budget annuale del 17%-25%.
Per affrontare i grandi investimenti iniziali spesso necessari per la vaccinazione, Gavi, la Vaccine Alliance, fornisce un cofinanziamento per le LMIC. Questi contributi del paese producono fino a 0,20 dollari per vaccino, con aumenti graduali fino a quando il paese non finanzia il vaccino in modo indipendente. Quando abbiamo ricalcolato l’ICER ipotizzando che Gavi coprisse il 25% del costo, l’ICER pagante è sceso da 678 dollari/valore a 158 dollari/valore. Se Gavi coprisse la metà del costo, l’ICER pagante diventerebbe negativo, indicando che l’intervento è un risparmio, ma i costi iniziali potrebbero non essere ancora accessibili per alcuni paesi.
Conclusione
La progettazione di un’assistenza sanitaria di alta qualità nell’era della copertura universale richiede informazioni sull’efficacia dei costi e sull’impatto del bilancio per i servizi sanitari in diversi contesti. Abbiamo scoperto che meno del 5% dei CEA sanitari mondiali conduce BIA. Con informazioni sia sull’efficacia dei costi che sull’impatto del budget, i responsabili politici possono sviluppare meglio una serie di programmi di alto valore per contesti specifici. Possono anche identificare servizi con costi elevati ma con alti benefici potenziali per la salute della popolazione per i quali cercare collaborazione o supporto finanziario esterno, in particolare i servizi di prevenzione e quelli che forniscono risparmi a lungo termine. Per promuovere l’effettiva incorporazione delle evidenze economiche nel processo decisionale, i ricercatori devono affrontare le lacune nei dati e comunicare chiaramente i risultati ai responsabili politici.
Al di là del valore economico, ci sono molte considerazioni aggiuntive nelle decisioni di budget, tra cui la necessità di identificare costi completi e accurati[46], bilanciare le priorità concorrenti [47], incorporare considerazioni di equità e di protezione finanziaria[48], e operare nei sistemi sanitari con più pagatori[16]. Tuttavia, accanto a questi fattori, una rigorosa considerazione sia del rapporto costo-efficacia che dell’accessibilità economica dovrebbero essere elementi chiave nella progettazione di pacchetti di servizi sanitari essenziali a livello globale.
Informazioni di supporto
References
- Goal 3: Ensure healthy lives and promote well-being for all at all ages. In: Sustainable Development Knowledge Platform [Internet]. [cited 28 Jun 2016]. Available:Publisher Full Text
- Boerma T, Eozenou P, Evans D, Evans T, Kieny M-P, Wagstaff A. Monitoring progress towards universal health coverage at country and global levels. PLoS Med. 2014; 11:e1001731. Publisher Full Text | PubMed
- Chalkidou K, Glassman A, Marten R, Vega J, Teerawattananon Y, Tritasavit N. Priority-setting for achieving universal health coverage. Bull World Health Organ. 2016; 94:462-467. Publisher Full Text | PubMed
- Teerawattananon Y, Luz A, Kanchanachitra C, Tantivess S. Role of priority setting in implementing universal health coverage. BMJ. 2016; 352:i244. Publisher Full Text | PubMed
- Summers LH. Economists’ declaration on universal health coverage. Lancet. 2015; 386:2112-2113. Publisher Full Text | PubMed
- Liu S, Watcha D, Holodniy M, Goldhaber-Fiebert JD. Sofosbuvir-based treatment regimens for chronic, genotype 1 hepatitis C virus infection in U.S. incarcerated populations: a cost-effectiveness analysis. Ann Intern Med. 2014; 161:546-553. Publisher Full Text | PubMed
- Linas BP, Barter DM, Morgan JR, Pho MT, Leff JA, Schackman BR. The cost-effectiveness of sofosbuvir-based regimens for treatment of hepatitis C virus genotype 2 or 3 infection. Ann Intern Med. 2015; 162:619. Publisher Full Text | PubMed
- Aggarwal R, Chen Q, Goel A, Seguy N, Pendse R, Ayer T. Cost-effectiveness of hepatitis C treatment using generic direct-acting antivirals available in India. PLoS ONE. 2017; 12:e0176503. Publisher Full Text | PubMed
- Urrutia J, Porteny T, Daniels N. What does it mean to put new hepatitis C drugs on a list of essential medicines?. BMJ. 2016; 353:i2035. Publisher Full Text | PubMed
- Iyengar S, Tay-Teo K, Vogler S, Beyer P, Wiktor S, Joncheere K de. Prices, Costs, and affordability of new medicines for hepatitis C in 30 countries: An economic analysis. PLoS Med. 2016; 13:e1002032. Publisher Full Text | PubMed
- Andrus JK, Jauregui B, Oliveira LHD, Matus CR. Challenges to building capacity For evidence-based new vaccine policy in developing countries. Health Aff (Millwood). 2011; 30:1104-1112. Publisher Full Text | PubMed
- Kim JJ, Campos NG, O’Shea M, Diaz M, Mutyaba I. Model-Based Impact and Cost-Effectiveness of Cervical Cancer Prevention in Sub-Saharan Africa. Vaccine. 2013; 31(Supplement 5):F60-F72. Publisher Full Text | PubMed
- Langley I, Lin H-H, Squire SB. Cost-effectiveness of Xpert MTB/RIF and investing in health care in Africa. Lancet Glob Health. 2015; 3:e83-e84. Publisher Full Text | PubMed
- Menzies NA, Cohen T, Lin H-H, Murray M, Salomon JA. Population Health Impact and Cost-Effectiveness of Tuberculosis Diagnosis with Xpert MTB/RIF: A Dynamic Simulation and Economic Evaluation. PLoS Med. 2012; 9:e1001347. Publisher Full Text | PubMed
- ICER Value Assessment Framework–ICER [Internet]. [cited 3 May 2016]. Available:Publisher Full Text
- Wiseman V, Mitton C, Doyle-Waters MM, Drake T, Conteh L, Newall AT. Using Economic Evidence to Set Healthcare Priorities in Low-Income and Lower-Middle-Income Countries: A Systematic Review of Methodological Frameworks. Health Econ. 2016; 25:140-161. Publisher Full Text | PubMed
- Sullivan SD, Mauskopf JA, Augustovski F, Jaime Caro J, Lee KM, Minchin M. Budget Impact Analysis—Principles of Good Practice: Report of the ISPOR 2012 Budget Impact Analysis Good Practice II Task Force. Value Health. 2014; 17:5-14. Publisher Full Text | PubMed
- Marshall DA, Douglas PR, Drummond MF, Torrance GW, Macleod S, Manti O. Guidelines for conducting pharmaceutical budget impact analyses for submission to public drug plans in Canada. PharmacoEconomics. 2008; 26:477-495. PubMed
- Care SB. Guidance on Budget Impact Analysis of Health Technologies in Ireland. 2015; Available:Publisher Full Text
- van de Vooren K, Duranti S, Curto A, Garattini L. A Critical Systematic Review of Budget Impact Analyses on Drugs in the EU Countries. Appl Health Econ Health Policy. 2013; 12:33-40. Publisher Full Text | PubMed
- NICE International (2014). Bill & Melinda Gates Foundation. Methods for Economic Evaluation Project (MEEP) Final Report.
- Neumann PJ, Thorat T, Zhong Y, Anderson J, Farquhar M, Salem M. A Systematic Review of Cost-Effectiveness Studies Reporting Cost-per-DALY Averted. PLoS ONE. 2016; 11:e0168512. Publisher Full Text | PubMed
- Jeuland M, Cook J, Poulos C, Clemens J, Whittington D. DOMI Cholera Economics Study Group. Cost-effectiveness of new-generation oral cholera vaccines: a multisite analysis. Value Health J Int Soc Pharmacoeconomics Outcomes Res. 2009; 12:899-908. Publisher Full Text | PubMed
- Niëns LM, Zelle SG, Gutiérrez-Delgado C, Rivera Peña G, Hidalgo Balarezo BR, Rodriguez Steller E. Cost-effectiveness of breast cancer control strategies in Central America: the cases of Costa Rica and Mexico. PLoS ONE. 2014; 9:e95836. Publisher Full Text | PubMed
- Basu S, Bendavid E, Sood N. Health and Economic Implications of National Treatment Coverage for Cardiovascular Disease in India. Circ Cardiovasc Qual Outcomes. 2015; 8:541-551. Publisher Full Text | PubMed
- Aguilar IBM, Mendoza LO, García O, Díaz I, Figueroa J, Duarte RM. Cost-effectiveness analysis of the introduction of the human papillomavirus vaccine in Honduras. Vaccine. 2015; 33(Supplement 1):A167-A173. Publisher Full Text | PubMed
- Strand KB, Chisholm D, Fekadu A, Johansson KA. Scaling-up essential neuropsychiatric services in Ethiopia: a cost-effectiveness analysis. Health Policy Plan. 2016; 31:504-513. Publisher Full Text | PubMed
- Ortega O, El-Sayed N, Sanders JW, Abd-Rabou Z, Antil L, Bresee J. Cost-Benefit Analysis of a Rotavirus Immunization Program in the Arab Republic of Egypt. J Infect Dis. 2009; 200:S92-S98. Publisher Full Text | PubMed
- Kim S-Y, Sweet S, Slichter D, Goldie SJ. Health and economic impact of rotavirus vaccination in GAVI-eligible countries. BMC Public Health. 2010; 10:253. Publisher Full Text | PubMed
- Goodman CA, Mutemi WM, Baya EK, Willetts A, Marsh V. The cost-effectiveness of improving malaria home management: shopkeeper training in rural Kenya. Health Policy Plan. 2006; 21:275-288. Publisher Full Text | PubMed
- Claxton K, Martin S, Soares M, Rice N, Spackman E, Hinde S. University of York, Centre for Health Economics; 2013. Publisher Full Text
- Dieleman JL, Templin T, Sadat N, Reidy P, Chapin A, Foreman K. National spending on health by source for 184 countries between 2013 and 2040. Lancet. 2016; 387:2521-2535. Publisher Full Text | PubMed
- Kuznik A, Lamorde M, Nyabigambo A, Manabe YC. Antenatal Syphilis Screening Using Point-of-Care Testing in Sub-Saharan African Countries: A Cost-Effectiveness Analysis. PLoS Med. 2013; 10Publisher Full Text | PubMed
- Drummond MF, Sculpher MJ, Torrance GW, O’Brien BJ, Stoddart GL. Methods for the Economic Evaluation of Health Care Programmes. Oxford University Press; 2005.
- Weinstein MC, Siegel JE, Gold MR, Kamlet MS, Russell LB. Recommendations of the Panel on Cost-effectiveness in Health and Medicine. JAMA. 1996; 276:1253-1258. PubMed
- Ahmeti A, Preza I, Simaku A, Nelaj E, Clark AD, Felix Garcia AG. Cost-effectiveness of rotavirus vaccination in Albania. Vaccine. 2015; 33(Supplement 1):A201-A208. Publisher Full Text | PubMed
- Andrieux-Meyer I, Cohn J, de Araújo ESA, Hamid SS. Disparity in market prices for hepatitis C virus direct-acting drugs. Lancet Glob Health. 2015; 3:e676-e677. Publisher Full Text | PubMed
- World Hepatitis Summit; 2015. Publisher Full Text
- Barua S, Greenwald R, Grebely J, Dore GJ, Swan T, Taylor LE. Restrictions for Medicaid Reimbursement of Sofosbuvir for the Treatment of Hepatitis C Virus Infection in the United States. Ann Intern Med. 2015; 163:215. Publisher Full Text | PubMed
- Brouwer WBF, Niessen LW, Postma MJ, Rutten FFH. Need for differential discounting of costs and health effects in cost effectiveness analyses. BMJ. 2005; 331:446-448. Publisher Full Text | PubMed
- Shiroiwa T, Sung Y-K, Fukuda T, Lang H-C, Bae S-C, Tsutani K. International survey on willingness-to-pay (WTP) for one additional QALY gained: what is the threshold of cost effectiveness?. Health Econ. 2010; 19:422-437. Publisher Full Text | PubMed
- Quentin W, Terris-Prestholt F, Changalucha J, Soteli S, Edmunds WJ, Hutubessy R. Costs of delivering human papillomavirus vaccination to schoolgirls in Mwanza Region, Tanzania. BMC Med. 2012; 10:137. Publisher Full Text | PubMed
- Campos NG, Sharma M, Clark A, Kim JJ, Resch SC. Resources Required for Cervical Cancer Prevention in Low- and Middle-Income Countries. PLoS ONE. 2016; 11:e0164000. Publisher Full Text | PubMed
- Fesenfeld M, Hutubessy R, Jit M. Cost-effectiveness of human papillomavirus vaccination in low and middle income countries: A systematic review. Vaccine. 2013; 31:3786-3804. Publisher Full Text | PubMed
- WHO. WHO. Publisher Full Text
- Cunnama L, Sinanovic E, Ramma L, Foster N, Berrie L, Stevens W. Using Top-down and Bottom-up Costing Approaches in LMICs: The Case for Using Both to Assess the Incremental Costs of New Technologies at Scale. Health Econ. 2016; 25:53-66. Publisher Full Text | PubMed
- Baltussen R, Jansen MP, Mikkelsen E, Tromp N, Hontelez J, Bijlmakers L. Priority setting for universal health coverage: We need evidence-informed deliberative processes, not just more evidence on cost-effectiveness. Int J Health Policy Manag. 2016. Publisher Full Text
- Verguet S, Laxminarayan R, Jamison DT. Universal Public Finance of Tuberculosis Treatment in India: An Extended Cost-Effectiveness Analysis. Health Econ. 2015; 24:318-332. Publisher Full Text | PubMed
Fonte
Bilinski A, Neumann P, Cohen J, Thorat T, McDaniel K, et al. (2017) When cost-effective interventions are unaffordable: Integrating cost-effectiveness and budget impact in priority setting for global health programs. PLoS Medicine 14(10): e1002397. https://doi.org/10.1371/journal.pmed.1002397





