Introduzione
Le cure ad alta intensità alla fine della vita hanno il potenziale di essere discordanti con le preferenze del paziente e non benefiche.1,2,3 Pertanto, sia il ricorso alla terapia intensiva durante gli ultimi 30 giorni di vita che la morte in terapia intensiva sono considerati indicatori negativi della qualità delle cure di fine vita.4 Inoltre, sebbene la percentuale di pazienti che muoiono a casa e la percentuale di pazienti che ricorrono all’hospice siano aumentate nel tempo, è aumentato anche il ricorso ai servizi di terapia intensiva nell’ultimo mese di vita, suggerendo che il ricorso a diversi tipi di misure di sostegno alla fine della vita può semplicemente aumentare.5 Diverse organizzazioni, tra cui l’Istituto di Medicina e la Campagna Scelta della Saggezza,6,7,8 hanno sostenuto l’aumento dell’uso delle cure palliative per mitigare l’elevata intensità del trattamento e migliorare la discrepanza tra le cure che i pazienti desiderano e le cure che ricevono effettivamente. Sebbene i programmi di cure palliative abbiano continuato ad espandersi a livello nazionale,9 non è noto se questa crescita sia associata a riduzioni dell’intensità del trattamento alla fine della vita. Pertanto, l’obiettivo di questo studio è stato quello di valutare se l’implementazione dei servizi di cure palliative ospedaliere è associata ad una successiva diminuzione dell’uso di cure intensive durante i ricoveri ospedalieri terminali.
Metodi
Pazienti e raccolta dati
Il protocollo dello studio è stato rivisto e approvato dal comitato di revisione istituzionale del Columbia University Medical Center. Si è rinunciato al consenso informato scritto. Poiché i dati sono stati deidentificati, la ricerca è stata giudicata a rischio minimo per i partecipanti e la rinuncia non avrebbe avuto effetti negativi sui diritti e sul benessere dei partecipanti. Questo studio di coorte aderisce alla linea guida per il rafforzamento della segnalazione degli studi osservazionali in epidemiologia(STROBE).10
I dati per questo studio provengono da un database a livello di paziente del New York Statewide Statewide Planning and Research Cooperative System e da una raccolta di caratteristiche a livello ospedaliero dell’American Hospital Association Annual Survey; le informazioni sui programmi di cure palliative provengono dal National Palliative Care Registry per gli anni dal 2008 al 2014. I dettagli sulla creazione di questo set di dati sono stati pubblicati in precedenza.11 Le analisi dei dati per questo studio sono state effettuate tra gennaio 2018 e luglio 2019.
L’esposizione primaria per questo studio è stata l’implementazione di un programma di cure palliative ospedaliere. Abbiamo scelto di utilizzare questo approccio per diversi motivi: (1) l’uso di un’esposizione a livello di paziente può essere più soggetto a distorsioni di indicazione rispetto a un’esposizione a livello ospedaliero; (2) con un’esposizione a livello di paziente, non avremmo informazioni sui tempi di consultazione delle cure palliative, il che potrebbe rendere i risultati difficili da interpretare in termini di temporalità; e (3) la ricezione delle cure palliative a livello di paziente non può essere determinata con precisione dai dati a livello di popolazione in questo momento.12 Abbiamo incluso gli ospedali che hanno sviluppato un programma di cure palliative durante il periodo di studio, così come gli ospedali che non hanno mai avuto un programma di cure palliative come controlli. Sono stati esclusi gli ospedali che hanno sempre avuto un programma di cure palliative durante il periodo di studio. Per ridurre gli errori di classificazione, per gli ospedali che hanno implementato un programma di cure palliative durante il periodo di studio, abbiamo escluso i dati di quell’ospedale per l’anno in cui il programma è stato istituito e per l’anno successivo, sia per consentire la penetrazione del programma all’interno dell’ospedale sia perché non avevamo informazioni su quando durante l’anno in cui il programma è stato avviato. Inoltre, gli ospedali che hanno sviluppato un programma di cure palliative durante il primo anno del periodo di studio (2008) o gli ultimi 2 anni (2013 e 2014) sono stati esclusi, perché non avevano dati di base o di follow-up sufficienti. Abbiamo anche escluso gli ospedali di piccole dimensioni (<100 posti letto) e gli ospedali rurali per ridurre l’eterogeneità delle caratteristiche ospedaliere, così come gli ospedali in cui meno dell’1% di tutti i ricoveri annuali ha ricevuto cure intensive, in media nel periodo di studio.
Abbiamo incluso tutti i pazienti di età pari o superiore ai 18 anni deceduti durante un ricovero terminale nello Stato di New York negli ospedali interessati. Abbiamo escluso i pazienti con precedenti di decessi multipli o con identificatori mancanti. Le covariate a livello di paziente disponibili all’interno del sistema cooperativo di pianificazione e ricerca dello Stato comprendevano l’età, il sesso, la razza, il tipo di assicurazione, la residenza urbana, il tipo di paziente (non chirurgico o chirurgico), il numero di comorbidità di Elixhauser,13 diagnosi di sepsi,14 rischio di mortalità e anno di ammissione. L’indicatore del rischio di mortalità all’interno del sistema cooperativo di pianificazione e ricerca in tutto lo Stato è calcolato utilizzando un software proprietario di raggruppamento sviluppato da 3M Health Information Systems che è integrato nel set di dati e si basa su età, comorbilità, procedure e diagnosi principale per il ricovero. Le variabili a livello ospedaliero dell’American Hospital Association Annual Survey comprendevano lo stato di insegnamento dell’ospedale, il numero di posti letto, il numero totale di ricoveri, il numero di procedure chirurgiche e il numero di equivalenti a tempo pieno di medici e infermieri, corretti per il numero di posti letto dell’ospedale; le variabili sono state confrontate utilizzando i dati dell’American Hospital Association corrispondenti all’anno di ricovero del paziente (per ulteriori dettagli sulle covariate, vedere l’appendice nel supplemento ).
Risultati
Il risultato principale di questo studio è stato l’accoglienza in terapia intensiva, definita come l’accoglienza in un’unità di terapia intensiva (ICU) (in base al fatto di avere una tariffa per l’utilizzo del letto ICU). I pazienti con spese intermedie di terapia intensiva non sono stati classificati come pazienti che hanno ricevuto cure intensive. Gli esiti secondari comprendevano la durata della degenza ospedaliera, l’uso della dialisi, i giorni in terapia intensiva (in base al numero di tariffe per l’utilizzo del letto in terapia intensiva) e l’uso della ventilazione meccanica per i pazienti ricoverati in terapia intensiva durante il ricovero.
Analisi statistica
Abbiamo riassunto le caratteristiche degli ospedali che hanno implementato o meno le cure palliative; abbiamo anche riassunto le caratteristiche demografiche e cliniche e calcolato le differenze standardizzate per i pazienti che hanno ricevuto cure in ospedali con e senza programmi di cure palliative. Abbiamo valutato l’associazione tra l’implementazione delle cure palliative ospedaliere e i risultati utilizzando un approccio basato sulle differenze e la regressione multilivello, modellando l’ospedale come un effetto casuale. Il modello delle differenze nelle differenze confronta il cambiamento dei risultati prima e dopo l’implementazione delle cure palliative negli ospedali che hanno istituito un programma con il cambiamento dei risultati negli ospedali che non hanno mai avuto un programma di cure palliative nello stesso periodo; questo modello stima l’associazione tra l’implementazione di un programma di cure palliative e i risultati dei pazienti durante i ricoveri terminali, adattandosi alle tendenze secolari. Per tenere conto del fatto che gli ospedali non hanno implementato tutti i programmi di cure palliative contemporaneamente, abbiamo specificato un modello che consente di variare i tempi di un intervento (vedere l’appendice nel supplemento per ulteriori dettagli).15 L’ipotesi di tendenza parallela è stata verificata per tutti i risultati utilizzando l’ispezione visiva (eFigure nel supplemento). Per tutte le analisi, la regressione logistica è stata utilizzata per modellare gli esiti binari non comuni (cioè quelli che si verificano con frequenza <10%), la regressione di Poisson con una robusta varianza di errore è stata utilizzata per gli esiti binari comuni (cioè quelli che si verificano con frequenza ≥10%),16 e la regressione binomiale negativa è stata usata per i risultati ordinali. Poiché l’esposizione primaria di interesse era una variabile a livello ospedaliero, abbiamo eseguito un centraggio di grande significato per le covariate a livello del paziente.17 Nei modelli di regressione, abbiamo incluso a priori l’età del singolo paziente, il sesso, la razza e il rischio di mortalità durante il ricovero come fattori di confusione, così come l’anno di ricovero ed eventuali variabili aggiuntive del paziente o dell’ospedale che avevano una differenza standardizzata maggiore di 0,1.18 Per l’analisi primaria, il P<0,05 su due lati è stato considerato statisticamente significativo. Il test χ 2 è stato utilizzato per testare la differenza non regolata tra l’utilizzo in terapia intensiva prima e dopo l’implementazione negli ospedali di implementazione. Dato il numero di risultati testati nelle analisi secondarie, abbiamo utilizzato una correzione Bonferroni per ridurre la probabilità di errore di tipo I, con il risultato che la soglia di significatività statistica è stata fissata a P=.002.
Analisi secondarie
A priori, abbiamo pianificato diverse analisi secondarie. Per affrontare le grandi differenze nelle caratteristiche ospedaliere, abbiamo ripetuto l’analisi delle differenze, stratificando per stato di insegnamento e numero di letti ospedalieri. Inoltre, poiché abbiamo usato un’esposizione a livello ospedaliero a una ricezione approssimativa di cure palliative specialistiche a livello di paziente, abbiamo ripetuto la nostra analisi in un’analisi di sottogruppo di pazienti con diagnosi di cancro metastatico (identificato usando l’algoritmo di codifica dell’indice di comorbidità di Elixhauser),13 perché questo rappresenta una popolazione di pazienti che ha potenzialmente maggiori probabilità di aver ricevuto un consulto per le cure palliative durante il ricovero in ospedale, se questi servizi fossero disponibili. Infine, abbiamo effettuato un’analisi post hoc, adeguando il numero di posti letto in terapia intensiva all’interno dell’ospedale, data l’evidenza che il ricorso alla terapia intensiva può variare a seconda dell’offerta.3,19 Il numero di posti letto in terapia intensiva è stato accertato utilizzando i dati dell’American Hospital Association Annual Survey per ogni ospedale per ogni anno; i pazienti curati in ospedali per i quali non erano disponibili tali informazioni sono stati esclusi da questa analisi (per i dettagli, vedere eAppendice nel supplemento). La gestione del database e l’analisi statistica sono state effettuate utilizzando il software statistico SAS versione 9.4 (SAS Institute) e il software statistico Stata versione 13.1 (StataCorp).
Risultati
Caratteristiche dell’ospedale e del paziente
Nello Stato di New York dal 2008 al 2014, 24 ospedali hanno attuato un programma durante il periodo di studio e 27 non hanno mai avuto un programma; ci sono stati 83 ospedali che hanno sempre avuto un programma di cure palliative per tutti gli anni e sono stati esclusi. Gli ospedali che hanno implementato le cure palliative in ambito ospedaliero hanno avuto più probabilità di avere uno status di insegnamento rispetto agli ospedali che non hanno mai avuto un programma (14 ospedali [58,3%] vs 11 ospedali [40,7%]), di avere 400 o più posti letto (5 ospedali [20,8%] vs 2 ospedali [7].4%]), e di avere un numero maggiore di ricoveri annuali (mediana [intervallo interquartile {IQR}], 13-161 [8427-19-102] ricoveri vs 7761 [4920-11171] ricoveri), operazioni chirurgiche (mediana [IQR], 8465 [6048-13].594] interventi contro 7018 [4181-8654] interventi), e medici a pieno carico (mediana [IQR], 27 [8-59] medici contro 22 [7-49] medici) e infermieri (mediana [IQR], 397 [251-591] infermieri contro 244 [161-411] infermieri)(Tabella 1). In questi ospedali, 73-370 pazienti (età media [SD], 76,5 [14,1] anni; 38-467 donne [52,4%]) hanno avuto un ricovero ospedaliero durante il quale sono morte (Figura);37-628 pazienti (51,3%) hanno ricevuto cure in ospedali che hanno implementato cure palliative, e 35-742 (48,7%) hanno ricevuto cure in un ospedale senza implementazione. Per i pazienti negli ospedali che hanno implementato l’implementazione, 17-146 pazienti (45,6%) hanno ricevuto cure prima dell’implementazione, e 20-482 (54,5%) hanno ricevuto cure dopo l’implementazione. Nel complesso, i pazienti curati negli ospedali che hanno implementato le cure palliative erano più giovani (età media [SD], 75,7 [14,5] anni contro 77,4 [13,6] anni) e più probabilmente di razza nera (6355 pazienti [16,9%] contro 3229 [9,0%]), vivono in un’area urbana (22-362 pazienti [59].4%] vs 16-202 pazienti [45,3%]), hanno un’assicurazione privata (8426 pazienti [22,4%] vs 6250 pazienti [17,5%]) e ricevono una diagnosi di sepsi durante il ricovero (20-878 pazienti [55,5%] vs 17877 pazienti [50,0%]) (Tabella 2).
| Caratteristica | Attuazione delle cure palliative ospedaliere, Ospedali, n. (%) | |
|---|---|---|
| No (n=27) | Sì (n = 24) | |
| Ospedale universitarioa | 11 (40.7) | 14 (58.3) |
| Letti, No.b | ||
| 100-399 | 25 (92.6) | 19 (79.2) |
| ≥400 | 2 (7.4) | 5 (20.8) |
| Ricoveri ospedalieri complessivi in terapia intensiva, mediana (IQR), %.b | 10 (7-14) | 9 (7-12) |
| Da 1 a <5 | 1 (3.7) | 2 (8.3) |
| Da 5 a <7 | 6 (22.2) | 3 (12.5) |
| Da 7 a <10 | 4 (14.8) | 9 (37.5) |
| 10 a <15 | 11 (40.7) | 8 (33.3) |
| Da 15 a <20 | 1 (3.7) | 0 |
| ≥20 | 4 (14.8) | 2 (8.3) |
| Ammissioni totali, mediana (IQR), n.b | 7761 (4920-11 171) | 13 161 (8427-19 102) |
| Totale operazioni chirurgiche, mediana (IQR), n.b | 7018 (4181-8654) | 8465 (6048-13 594) |
| Medici e dentisti equivalenti a tempo pieno, mediano (IQR), No.b | 22 (7-49) | 27 (8-59) |
| Infermieri registrati equivalenti a tempo pieno, mediana (IQR), n.b | 244 (161-411) | 397 (251-591) |
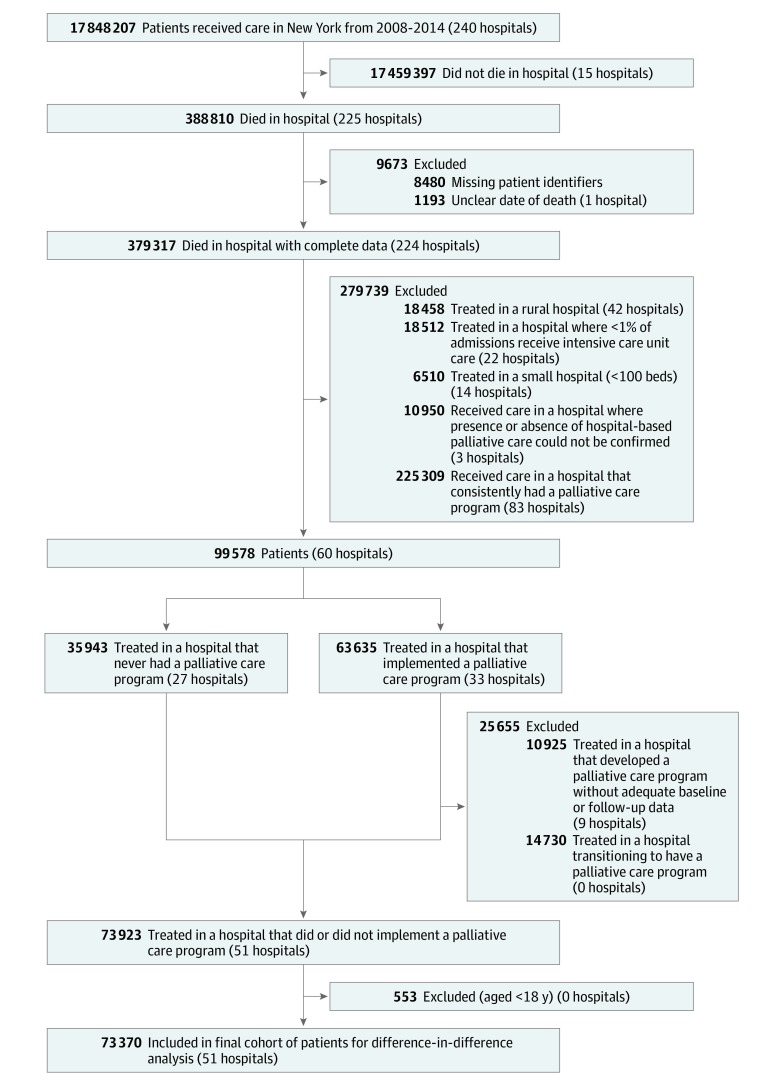
Figura.Diagramma di flusso della creazione della coorteIl diagramma di flusso mostra i criteri di inclusione ed esclusione per gli ospedali e i pazienti della coorte di studio.
| Caratteristica | Attuazione delle cure palliative ospedaliere, pazienti, n. (%) | Differenza standardizzata | |
|---|---|---|---|
| No (n = 35-742) | Sì (n=37-628) | ||
| Età, media (SD), y | 77.4 (13.6) | 75.7 (14.5) | |
| Fascia di età, y | |||
| 18-64 | 6169 (17.3) | 8063 (21.4) | 0.12 |
| 65-74 | 6278 (17.6) | 6903 (18.4) | |
| 75-84 | 10 595 (29.6) | 10 616 (28.2) | |
| ≥85 | 12 700 (35.5) | 12 046 (32.0) | |
| Sesso | |||
| Femmina | 18 880 (52.8) | 19 587 (52.1) | –0.02 |
| Maschio | 16 862 (47.2) | 18 041 (48.0) | |
| Gara | |||
| Bianco | 27 386 (76.6) | 25 362 (67.0) | 0.25 |
| Nero | 3229 (9.0) | 6355 (16.9) | |
| Altro | 5019 (14.0) | 5626 (15.0) | |
| Residenza di campagna | |||
| Urbano | 16 202 (45.3) | 22 362 (59.4) | 0.33 |
| Misto | 17 176 (48.1) | 14 363 (38.2) | |
| Rurale | 2224 (6.2) | 731 (1.9) | |
| Assicurazione | |||
| Medicare | 24855 (69.5) | 25 216 (67.0) | 0.20 |
| Medicaid | 1492 (4.2) | 1977 (5.3) | |
| Privato | 6250 (17.5) | 8426 (22.4) | |
| Auto-pagamento | 2532 (7.1) | 1306 (3.5) | |
| Altro | 613 (1.7) | 703 (1.9) | |
| Chirurgico | 5088 (14.2) | 6506 (17.3) | 0.08 |
| N. di comorbidità di Elixhauser | |||
| 0 | 1018 (2.9) | 1246 (3.3) | 0.04 |
| 1-3 | 15 076 (42.2) | 16 327 (43.4) | |
| ≥4 | 19 648 (55.0) | 20 055 (53.3) | |
| Rischio di mortalità all’inizio del ricovero ospedalieroa | |||
| Minorenne | 485 (1.4) | 565 (1.5) | 0.096 |
| Moderato | 3310 (9.3) | 3071 (8.2) | |
| Maggiore | 10 922 (30.6) | 10 172 (27.0) | |
| Estremo | 21025 (58.8) | 23 820 (63.3) | |
| Sepsib | 17 877 (50.0) | 20 878 (55.5) | 0.11 |

Figura.Diagramma di flusso della creazione della coorteIl diagramma di flusso mostra i criteri di inclusione ed esclusione per gli ospedali e i pazienti della coorte di studio.
Attuazione delle cure palliative e ammissione in terapia intensiva
Il ricovero in terapia intensiva durante un ricovero ospedaliero terminale è stato frequente (50,9% per i pazienti curati in ospedali che hanno implementato cure palliative ospedaliere contro il 46,0% per i pazienti in ospedali che non lo hanno fatto). I pazienti che hanno ricevuto cure in un ospedale dopo l’implementazione delle cure palliative hanno avuto meno probabilità di ricevere cure intensive rispetto ai pazienti in quegli stessi ospedali prima dell’implementazione (49,3% dopo vs 52,8% prima; differenza 3,5%; 95% IC, 2,5%-4,5%; P<<.001). Rispetto agli ospedali che non hanno mai avuto un programma di cure palliative, l’implementazione delle cure palliative è stata associata ad una riduzione del 10% dell’uso di TI durante i ricoveri terminali (rischio relativo corretto [aRR], 0,90; 95% di IC, 0,85-0,95; P  P<<<.001) (Tabella 3). L’implementazione delle cure palliative ospedaliere non è stata associata a differenze significative nella durata della degenza ospedaliera (mediana [IQR], 6 [2-13] giorni contro 7 [2-15] giorni; rapporto di tasso corretto, 1,03; 95% di IC, 1,00-1,06) o all’uso della dialisi (8,8% dei pazienti contro 9,4% dei pazienti; rapporto di probabilità corretto, 0.94; 95% IC, 0,82-1,07), o con differenze nei giorni di terapia intensiva (mediana [IQR], 4 [2-9] giorni contro 5 [2-10] giorni; rapporto di frequenza regolato, 0,96; 95% IC, 0,91-1,01) o uso della ventilazione meccanica (68,5% dei pazienti contro 69,2% dei pazienti; rischio relativo regolato, 0,96; 95% IC, 0,92-1,01) per i pazienti ricoverati in terapia intensiva(Tabella 3).
| Risultato | Implementazione delle cure palliative ospedaliere, risultati non corretti | Estimatore delle differenze (95% CI)a | P Valore | ||
|---|---|---|---|---|---|
| Sì (n=37-628) | No (n = 35-742) | ||||
| Prima di | Dopo | ||||
| Risultato primario, utilizzo in terapia intensiva, %.b | 52.8 | 49.3 | 46.0 | 0.90 (0.85-0.95) | <.001 |
| Risultati secondari | |||||
| Dialisi, %.c | 9.4 | 8.8 | 7.0 | 0.94 (0.82-1.07) | .34 |
| Durata della degenza ospedaliera, mediana (IQR), dd | 7 (2-15) | 6 (2-13) | 6 (2-13) | 1.03 (1.00-1.06) | .09 |
| Ventilazione meccanica, %.b,e | 69.2 | 68.5 | 59.5 | 0.96 (0.92-1.01) | .12 |
| Utilizzo del letto per terapia intensiva, mediana (IQR), dd,e | 5 (2-10) | 4 (2-9) | 4 (1-8) | 0.96 (0.91-1.01) | .09 |
Analisi secondarie
Per le analisi stratificate per caratteristiche ospedaliere, l’associazione tra l’implementazione delle cure palliative ospedaliere e il ricovero in terapia intensiva è stata limitata agli ospedali didattici (aRR, 0,81; 95% CI, 0,74-0,88; P<-001) e ai grandi ospedali con 400 o più letti (aRR, 0,88; 95% CI, 0,83-0,94; P<-001) . L’implementazione delle cure palliative è stata anche associata ad una diminuzione del numero di giorni di terapia intensiva per i pazienti ricoverati in terapia intensiva negli ospedali didattici (aRR, 0,87; 95% IC, 0,82-0,93; P</ 001) e nei grandi ospedali con 400 letti o più (aRR, 0,78; 95% IC, 0,66-0,91; P=.002) (Tabella 4).
| Risultato | Tipo di ospedale | Numero letto | Pazienti con cancro metastatico (n = 10-177) | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Non insegnamento (n=28-777) | Insegnamento (n = 44-593) | 100-399 (n = 54 621) | ≥400 (n = 18 749) | |||||||
| Estimatore (95% CI)a | P Valoreb | Estimatore (95% CI)c | P Valoreb | Estimatore (95% CI)d | P Valoreb | Estimatore (95% CI)e | P Valoreb | Estimatore (95% CI)f | P Valoreb | |
| Risultato primario, utilizzo in terapia intensiva, %.g | 1.00 (0.89-1.13) | .96 | 0.81 (0.74-0.88) | <.001 | 0.95 (0.88-1.03) | .18 | 0.88 (0.83-0.94) | <.001 | 0.76 (0.65-0.88) | <.001 |
| Risultati secondari | ||||||||||
| Dialisi, %.h | 0.89 (0.66-1.19) | .44 | 0.89 (0.75-1.05) | .16 | 1.00 (0.85-1.17) | .97 | 0.67 (0.45-1.00) | .049 | 0.86 (0.55-1.34) | .50 |
| Durata della permanenza, mediana (IQR), di | 1.13 (1.07-1.20) | <.001 | 0.95 (0.90-1.00) | .03 | 1.03 (0.99-1.08) | .10 | 0.98 (0.87-1.11) | .81 | 1.01 (0.93-1.10) | .85 |
| Ventilazione meccanica, %.g,j | 0.88 (0.65-1.18) | .38 | 0.98 (0.93-1.03) | .47 | 0.98 (0.93-1.04) | .56 | 1.00 (0.92-1.09) | .98 | 0.87 (0.62-1.21) | .41 |
| Utilizzo del letto per terapia intensiva, mediana (IQR), di,j | 1.11 (1.02-1.20) | .01 | 0.87 (0.82-0.93) | <.001 | 0.98 (0.93-1.04) | .58 | 0.78 (0.66-0.91) | .002 | 0.93 (0.81-1.06) | .29 |
Per il sottogruppo di 10-177 pazienti in condizioni critiche con cancro metastatico, c’è stata ancora una volta un’associazione tra l’implementazione delle cure palliative ospedaliere e una significativa diminuzione dell’uso di terapia intensiva durante i ricoveri terminali (adjusted odds ratio, 0,76; 95% CI, 0,65-0,88; P<<0,001) e nessuna differenza significativa negli esiti secondari (Tabella 4). Abbiamo ripetuto l’analisi primaria, tenendo conto del numero di posti letto in terapia intensiva presso l’ospedale. Dopo aver escluso i pazienti senza informazioni sul numero di posti letto in terapia intensiva, abbiamo incluso nell’analisi 71 506 pazienti di 48 ospedali. Dopo l’adeguamento per il numero di posti letto di terapia intensiva in un ospedale, i risultati sono rimasti invariati (eTable nel supplemento).
Discussione
Utilizzando un approccio basato sulle differenze, abbiamo scoperto che l’implementazione di un programma di cure palliative ospedaliere era associata ad una piccola ma misurabile diminuzione nell’uso della terapia intensiva durante i ricoveri ospedalieri terminali. Abbiamo trovato risultati simili per i pazienti con cancro metastatico, un sottogruppo di pazienti che avrebbero potuto ricevere un consulto per le cure palliative, perché i medici potrebbero essere più propensi a riconoscere che questi pazienti hanno una malattia terminale con una prognosi sfavorevole e perché ci sono prove a sostegno del beneficio delle cure palliative nei pazienti con cancro.20 Sebbene la differenza osservata sia stata piccola (diminuzione assoluta del 3,5%), a livello di popolazione, l’associazione può essere amplificata. Circa 2,8 milioni di persone sono morte negli Stati Uniti nel 2017,21 di cui si stima che il 15% sia morto in terapia intensiva.22 Un soggiorno in terapia intensiva ha un costo medio stimato di 10-811 dollari per i pazienti che muoiono,23 e l’uso delle unità di terapia intensiva è stimato aumentare i costi di ricovero di un terzo, con una differenza di costo di 2703 dollari tra i pazienti che utilizzano e non utilizzano l’unità di terapia intensiva durante un ricovero terminale.24 Con queste stime, una diminuzione dell’uso di TI del 3,5% si tradurrebbe in una differenza di costo di circa 265 milioni di dollari. Sebbene ciò fornisca una certa comprensione delle implicazioni dell’implementazione delle cure palliative per il sistema sanitario statunitense, è importante qualificare che questi dati non devono essere presi per indicare che una diminuzione dell’uso di TI si tradurrebbe in un aumento del valore delle cure. Dato che l’uso delle unità di terapia intensiva al termine della vita è comune, e studi recenti mettono in discussione il fatto che le cure di qualità al termine della vita debbano essere equiparate a cure meno intensive,25,26 può darsi che l’unità di terapia intensiva fornisca valore ai pazienti e alle famiglie in modo incompleto.
In analisi stratificate, abbiamo osservato che l’associazione dell’implementazione delle cure palliative ospedaliere non è coerente tra i diversi tipi di ospedali, con associazioni significative limitate all’insegnamento e ai grandi ospedali. Inoltre, in questi ospedali, l’implementazione delle cure palliative era anche associata ad una significativa diminuzione del numero di giorni in terapia intensiva per i pazienti ricoverati in terapia intensiva, suggerendo che l’associazione si estendeva oltre la semplice prevenzione del ricovero in terapia intensiva. In uno studio precedente,11 Abbiamo anche osservato una tale eterogeneità di associazioni, con la disponibilità di cure palliative ospedaliere associate a un aumento delle dimissioni in hospice per i pazienti in condizioni critiche solo nell’insegnamento e nei grandi ospedali. Le ragioni di questa eterogeneità non sono chiare, in particolare, se sia associata a differenze tra programmi di cure palliative, differenze tra ambienti ospedalieri e culture, o entrambe. È noto che i team di cure palliative hanno differenze sostanziali nelle loro caratteristiche operative, come la quantità di personale e la composizione del team di cure palliative.27,28,29 Queste differenze possono essere associate all’efficacia di un programma di cure palliative, perché l’aumento del personale è stato associato ad una maggiore penetrazione del servizio di cure palliative (definita dal numero di consulenze viste sul numero totale di ricoveri) e ad un tempo più breve per la consultazione iniziale.29,30 Inoltre, le culture ospedaliere possono seguire pratiche diverse, in particolare per quanto riguarda l’uso di terapie di mantenimento della vita e la fornitura di cure di fine vita.31,32,33 Tuttavia, nello studio attuale, mancano ulteriori dati dettagliati sui programmi di cure palliative o sulle pratiche ospedaliere e, quindi, non siamo in grado di valutare come questi fattori possano aver contribuito ai risultati osservati.
I nostri risultati sono in linea con quelli degli studi precedenti34,35,36,37,38 dimostrando che il ricorso al consulto per le cure palliative è associato a una minore probabilità di morte dei pazienti in terapia intensiva e a soggiorni più brevi in terapia intensiva per i pazienti deceduti durante il ricovero. A differenza di questi studi precedenti, che esaminavano l’uso della consultazione in ospedali con programmi di cure palliative esistenti, abbiamo utilizzato un approccio quasi sperimentale ed ecologico (l’analisi delle differenze nelle differenze) per valutare meglio l’associazione prevista tra l’implementazione di un programma di cure palliative in ospedale e i risultati. Inoltre, abbiamo utilizzato un ampio campione di ospedali con caratteristiche diverse che hanno permesso di esaminare come i risultati associati all’implementazione di un programma di cure palliative possano differire tra i diversi tipi di ospedali e di migliorare la generalizzabilità dei nostri risultati. Studi precedenti39,40,41 di approcci proattivi alla ricerca di casi concreti per aumentare l’erogazione di cure palliative hanno anche trovato un’associazione tra l’uso delle cure palliative e la diminuzione dell’uso di specifiche terapie non benefiche per la vita, che non abbiamo osservato. Ciò può essere dovuto al fatto che l’associazione tra la consultazione in cure palliative e la riduzione dell’uso di tali terapie dipende probabilmente dai tempi di inizio.42,43in 1 studio,44 l’associazione tra il consulto per le cure palliative e i costi di terapia intensiva non era significativa, a meno che il consulto non fosse iniziato entro 2 giorni dal ricovero in ospedale.
In combinazione con altri studi, i nostri risultati suggeriscono che la disponibilità di un consulto per le cure palliative può ridurre l’intensità del trattamento alla fine della vita. La morte meno medicamentosa è stata associata a valutazioni più elevate della qualità della vita, della qualità della morte e della qualità delle cure di fine vita45,46,47 e meno sintomi psicologici nelle persone in lutto, in particolare per i pazienti con cancro avanzato.48,49 Alla luce di questi dati, l’implementazione di programmi di cure palliative può essere un modo per migliorare la qualità delle cure di fine vita per alcuni pazienti che muoiono in ospedale.
Limitazioni
Il principale limite di questo studio è la possibilità di confusione residua; gli ospedali che hanno scelto di implementare programmi di cure palliative possono essere fondamentalmente diversi da quelli che non lo hanno fatto. Anche se abbiamo scoperto che gli ospedali hanno avuto una diminuzione nell’uso della terapia intensiva dopo l’implementazione delle cure palliative ospedaliere, il tasso complessivo di utilizzo di terapia intensiva era ancora sostanzialmente più alto in questi ospedali rispetto agli ospedali che non hanno mai implementato le cure palliative. Quindi, è possibile che gli ospedali che non hanno implementato le cure palliative avessero già messo in atto altri meccanismi per evitare l’uso di interventi ad alta intensità o di pratiche diverse che circondano le cure alla fine della vita. Abbiamo affrontato la possibilità di confusione a livello ospedaliero includendo caratteristiche ospedaliere multiple, tenendo conto delle differenze nei risultati di base utilizzando un modello a effetti casuali e conducendo un’analisi delle differenze nelle differenze per tenere conto delle tendenze secolari. Tuttavia, è ancora possibile che altre differenze nelle cure fornite tra gli ospedali possano rendere conto dei nostri risultati. Non siamo stati in grado di rendere conto delle differenze nell’uso effettivo delle consulenze per le cure palliative all’interno degli ospedali, perché non sono state rilevate con precisione all’interno dei dati amministrativi.12 Ci mancava anche la granularità dei dati per poter confermare i meccanismi alla base delle nostre scoperte, comprese le caratteristiche del team di cure palliative all’interno degli ospedali, come il personale e la disponibilità del team, così come i dettagli sulle cure di fine vita erogate o se i pazienti disponevano di direttive anticipate al momento del ricovero in ospedale. Anche se abbiamo eseguito un’analisi secondaria che si è adattata al numero di posti letto per le unità di terapia intensiva dell’ospedale, la reale disponibilità di posti letto per le unità di terapia intensiva dipende spesso da altri fattori che non erano a nostra disposizione, come i dettagli sul personale infermieristico e l’occupazione. Abbiamo dovuto escludere la maggior parte degli ospedali perché disponevano di programmi di cure palliative già esistenti, riducendo così la validità interna dei nostri risultati. Inoltre, New York è uno stato con un’intensità di trattamento relativamente alta rispetto ad altri stati, e questi risultati potrebbero non essere generalizzabili ad altre regioni degli Stati Uniti o di altri paesi.50 Inoltre, abbiamo utilizzato una coorte deceduta, perché gli indicatori di qualità per le cure di fine vita si concentrano sull’intensità delle cure fornite nell’immediato periodo che precede il decesso. Tuttavia, in prospettiva, non è chiaro quali pazienti moriranno e non è stato valutato l’impatto dell’introduzione delle cure palliative sui pazienti con patologie non terminali.
Conclusioni
Questi dati indicano che l’implementazione di programmi di cure palliative è associata ad una modesta diminuzione dell’uso della terapia intensiva durante i ricoveri ospedalieri terminali e che l’associazione può essere diversa a seconda delle caratteristiche dell’ospedale. Il lavoro futuro dovrebbe concentrarsi sull’identificazione delle caratteristiche associate all’efficacia dei programmi di cure palliative nel diminuire l’intensità del trattamento.
References
- Understanding the treatment preferences of seriously ill patients. N Engl J Med. 2002; 346(14)DOI | PubMed
- How often is end-of-life care in the United States inconsistent with patients’ goals of care?. J Palliat Med. 2017; 20(12):1400-1404. DOI | PubMed
- Association of increasing use of mechanical ventilation among nursing home residents with advanced dementia and intensive care unit beds. JAMA Intern Med. 2016; 176(12):1809-1816. DOI | PubMed
- 2009. Publisher Full Text
- Change in end-of-life care for Medicare beneficiaries: site of death, place of care, and health care transitions in 2000, 2005, and 2009. JAMA. 2013; 309(5):470-477. DOI | PubMed
- Dying in America: Improving Quality and Honoring Individual Preferences Near the End of Life. The National Academies Press: Washington, DC; 2014.
- Integrating palliative care in the ICU. Curr Opin Crit Care. 2014; 20(6):673-680. DOI | PubMed
- 2014. Publisher Full Text
- The growth of palliative care in U.S. hospitals: a status report. J Palliat Med. 2016; 19(1):8-15. DOI | PubMed
- The Strengthening the Reporting of Observational Studies in Epidemiology (STROBE) statement: guidelines for reporting observational studies. Ann Intern Med. 2007; 147(8):573-577. DOI | PubMed
- Association between the availability of hospital-based palliative care and treatment intensity for critically ill patients. Ann Am Thorac Soc. 2018; 15(9):1067-1074. DOI | PubMed
- Validation of the V66.7 code for palliative care consultation in a single academic medical center. J Palliat Med. 2017; 20(4):372-377. DOI | PubMed
- Comorbidity measures for use with administrative data. Med Care. 1998; 36(1):8-27. DOI | PubMed
- Epidemiology of severe sepsis in the United States: analysis of incidence, outcome, and associated costs of care. Crit Care Med. 2001; 29(7):1303-1310. DOI | PubMed
- Designing difference in difference studies: best practices for public health policy research. Annu Rev Public Health. 2018; 39(1):453-469. DOI | PubMed
- A modified Poisson regression approach to prospective studies with binary data. Am J Epidemiol. 2004; 159(7):702-706. DOI | PubMed
- Centering predictor variables in cross-sectional multilevel models: a new look at an old issue. Psychol Methods. 2007; 12(2):121-138. DOI | PubMed
- Interpreting estimates of treatment effects: implications for managed care. P T. 2008; 33(12):700-711. PubMed
- Effects of changes in ICU bed supply on ICU utilization. Med Care. 2019; 57(7):544-550. DOI | PubMed
- Early palliative care for patients with metastatic non-small-cell lung cancer. N Engl J Med. 2010; 363(8):733-742. DOI | PubMed
- 2019. Publisher Full Text
- 2014. Publisher Full Text
- The impact of mortality on total costs within the ICU. Crit Care Med. 2017; 45(9):1457-1463. DOI | PubMed
- Intensive care unit admission and survival among older patients with chronic obstructive pulmonary disease, heart failure, or myocardial infarction. Ann Am Thorac Soc. 2017; 14(6):943-951. DOI | PubMed
- End-of-life care received by physicians compared with nonphysicians. JAMA Netw Open. 2019; 2(7)DOI | PubMed
- How U.S. doctors die: a cohort study of healthcare use at the end of life. J Am Geriatr Soc. 2016; 64(5):1061-1067. DOI | PubMed
- Characteristics of palliative care consultation services in California hospitals. J Palliat Med. 2012; 15(5):555-560. DOI | PubMed
- Two steps forward, one step back: changes in palliative care consultation services in California hospitals from 2007 to 2011. J Palliat Med. 2014; 17(11):1214-1220. DOI | PubMed
- 2017. Publisher Full Text
- Impact of staffing on access to palliative care in U.S. hospitals. J Palliat Med. 2015; 18(12):998-999. DOI | PubMed
- Hospital end-of-life treatment intensity among cancer and non-cancer cohorts. J Pain Symptom Manage. 2015; 49(3):521-529. DOI | PubMed
- Advance care planning norms may contribute to hospital variation in end-of-life ICU use: a simulation study. Med Decis Making. 2014; 34(4):473-484. DOI | PubMed
- Norms of decision making in the ICU: a case study of two academic medical centers at the extremes of end-of-life treatment intensity. Intensive Care Med. 2012; 38(11):1886-1896. DOI | PubMed
- Palliative care consultation teams cut hospital costs for Medicaid beneficiaries. Health Aff (Millwood). 2011; 30(3):454-463. DOI | PubMed
- Cost savings associated with US hospital palliative care consultation programs. Arch Intern Med. 2008; 168(16):1783-1790. DOI | PubMed
- Proactive palliative care in the medical intensive care unit: effects on length of stay for selected high-risk patients. Crit Care Med. 2007; 35(6):1530-1535. DOI | PubMed
- Evidence-based palliative care in the intensive care unit: a systematic review of interventions. J Palliat Med. 2014; 17(2):219-235. DOI | PubMed
- Cost and utilization outcomes of patients receiving hospital-based palliative care consultation. J Palliat Med. 2006; 9(4):855-860. DOI | PubMed
- Preliminary report of the integration of a palliative care team into an intensive care unit. Palliat Med. 2010; 24(2):154-165. DOI | PubMed
- A proactive approach to improve end-of-life care in a medical intensive care unit for patients with terminal dementia. Crit Care Med. 2004; 32(9):1839-1843. DOI | PubMed
- Impact of a proactive approach to improve end-of-life care in a medical ICU. Chest. 2003; 123(1):266-271. DOI | PubMed
- The costs of waiting: implications of the timing of palliative care consultation among a cohort of decedents at a comprehensive cancer center. J Palliat Med. 2016; 19(1):69-75. DOI | PubMed
- The role and timing of palliative medicine consultation for women with gynecologic malignancies: association with end of life interventions and direct hospital costs. Gynecol Oncol. 2014; 132(1):3-7. DOI | PubMed
- Prospective cohort study of hospital palliative care teams for inpatients with advanced cancer: earlier consultation is associated with larger cost-saving effect. J Clin Oncol. 2015; 33(25):2745-2752. DOI | PubMed
- Comparing the quality of death for hospice and non-hospice cancer patients. Med Care. 1988; 26(2):177-182. DOI | PubMed
- Quality of end-of-life care provided to patients with different serious illnesses. JAMA Intern Med. 2016; 176(8):1095-1102. DOI | PubMed
- Family perspectives on aggressive cancer care near the end of life. JAMA. 2016; 315(3):284-292. DOI | PubMed
- Associations between end-of-life discussions, patient mental health, medical care near death, and caregiver bereavement adjustment. JAMA. 2008; 300(14):1665-1673. DOI | PubMed
- Place of death: correlations with quality of life of patients with cancer and predictors of bereaved caregivers’ mental health. J Clin Oncol. 2010; 28(29):4457-4464. DOI | PubMed
- 2014. Publisher Full Text
Fonte
Hua M, Lu Y, Ma X, Morrison RS, Li G, et al. (2020) Association Between the Implementation of Hospital-Based Palliative Care and Use of Intensive Care During Terminal Hospitalizations. JAMA Network Open 3(1): e1918675. https://doi.org/10.1001/jamanetworkopen.2019.18675





