
Introduzione
La tromboembolia venosa (TEV) è un importante problema di salute globale e una considerazione importante per i pazienti e i medici al momento della chirurgia elettiva. Prima degli interventi chirurgici elettivi, i pazienti vengono sottoposti a una valutazione del rischio di TEV per guidare l’uso di misure meccaniche e di farmacotromboprofilassi. Esistono prove dell’uso della farmacotromboprofilassi e delle calze a compressione graduata (GCS) come tromboprofilassi meccanica in questo gruppo di pazienti.1 Una revisione sistematica e una meta-analisi di 20 studi in pazienti chirurgici hanno dimostrato tassi molto più bassi di trombosi venosa profonda in pazienti randomizzati a GCS (134/1365, 9,8%) rispetto a quelli dei gruppi di controllo (282/1328, 21,2%)2; tuttavia, 19 di questi studi sono stati condotti prima dell’anno 2000. I tassi di TEV sono diminuiti negli ultimi 50 anni, in parte a causa della tromboprofilassi, ma anche a causa dei cambiamenti nella pratica clinica.3 Pertanto, l’efficacia della GCS nella pratica moderna è incerta. Nei pazienti chirurgici, l’uso di eparina a basso peso molecolare (LMWH) riduce i TEV clinici e i TEV senza sintomi.4 Le attuali linee guida raccomandano ampiamente la prevenzione del TEV in assenza di controindicazioni utilizzando una combinazione di GCS e di farmacotromboprofilassi per i pazienti sottoposti a chirurgia elettiva che sono a moderato o alto rischio di TEV. Nel Regno Unito, lo strumento di valutazione del rischio di TEV del Dipartimento della Salute è raccomandato(https://www.nice.org.uk/guidance/ng89/resources/department-of-health-vte-risk-assessment-tool-pdf-4787149213),5 mentre a livello internazionale, lo strumento di valutazione del rischio Caprini(https://venousdisease.com/caprini-dvt-risk-assessment/) è utilizzato anche per determinare il rischio di TEV dei pazienti.6
7
L’efficacia della GCS nella pratica moderna è stata messa in discussione.8 Un ampio studio randomizzato controllato in pazienti con ictus ha mostrato un aumento degli eventi avversi con la GCS senza un beneficio di accompagnamento nella riduzione del TEV.9 Nel contesto della chirurgia elettiva, una revisione sistematica10 ha identificato un solo studio in pazienti sottoposti a chirurgia ortopedica che ha valutato il beneficio della GCS in aggiunta alla farmacotromboprofilassi. Questo singolo studio non ha trovato alcun beneficio aggiuntivo nell’uso della GCS.11 La revisione ha concluso che il confronto quantitativo o l’elaborazione di conclusioni definitive era difficile.10
Abbiamo eseguito la compressione graduata in aggiunta allo studio di farmacotromboprofilassi in chirurgia (GAPS)12, uno studio ampio, pragmatico, multicentrico, di efficacia clinica, a due bracci, gruppo parallelo, randomizzato e controllato di non inferiorità. In questo studio abbiamo valutato l’aggiunta di GCS a LMWH per la prevenzione della TEV in pazienti sottoposti a chirurgia elettiva. Il nostro obiettivo era quello di indagare se la sola dose tromboprofilattica LMWH non fosse inferiore alla dose tromboprofilattica LMWH e GCS nella prevenzione della trombosi venosa profonda degli arti inferiori con o senza sintomi, o dell’embolia polmonare con sintomi fino a 90 giorni dopo l’intervento.
Metodi
Studio di progettazione
Tra il maggio 2016 e il gennaio 2019, abbiamo arruolato i partecipanti a questo studio clinico randomizzato non di inferiorità in sette centri in tutto il Regno Unito (appendice supplementare). I dettagli del progetto e dell’implementazione dello studio sono forniti nel protocollo, che è stato pubblicato in precedenza.12 Tutti i partecipanti hanno fornito il consenso informato per iscritto e un comitato direttivo dello studio e un comitato indipendente di monitoraggio dei dati ha fornito la supervisione dello studio.
I partecipanti
I pazienti di età pari o superiore ai 18 anni che si sottopongono a chirurgia elettiva e che sono stati valutati come a rischio moderato (punteggio 1) o ad alto rischio (punteggio ≥2) di TEV utilizzando lo strumento di valutazione del rischio di TEV del Dipartimento della Salute5 (figura supplementare, appendice 3 del web) sono stati sottoposti a screening per l’idoneità. Abbiamo anche valutato il rischio di TEV utilizzando lo strumento di valutazione del rischio Caprini per valutare l’applicabilità a livello mondiale.7 Abbiamo escluso le pazienti di sesso femminile se erano incinte, e le pazienti che avevano controindicato la LMWH o la GCS, se avevano una trombofilia o un disturbo trombotico, se necessitavano di anticoagulazione terapeutica o se avevano un’anamnesi di TEV. Abbiamo anche escluso i pazienti che richiedevano l’inserimento del filtro vena cava inferiore, la compressione pneumatica intermittente oltre l’area di recupero post anestesia, la tromboprofilassi estesa (oltre la scarica), o se avevano bisogno di un gesso o di un tutore da applicare in sala operatoria. Tutti i partecipanti hanno fornito il consenso informato per iscritto.
Modifiche al disegno dello studio
A causa del basso tasso di eventi (analisi in cieco su 1294 partecipanti) e dopo l’input del comitato direttivo dello studio e del comitato indipendente di monitoraggio dei dati, il disegno dello studio è stato rivisto nel dicembre 2017 (dettagli completi nel protocollo di studio e nell’appendice supplementare) per stratificare il reclutamento in base all’età (<65 o ≥65 anni) e al rischio di TEV (moderato o elevato). Abbiamo abbandonato il disegno sequenziale di gruppo e abbiamo specificato una non inferiorità appropriata per queste quattro sottopopolazioni. I risultati sono riportati per il campione originale non stratificato e il campione stratificato rivisto.
Randomizzazione e mascheramento
I partecipanti sono stati randomizzati 1:1 alla farmacotromboprofilassi con il solo LMWH o al LMWH e alla GCS prima dell’intervento. La randomizzazione è stata effettuata attraverso un’applicazione basata sul web ospitata dal Centro per le sperimentazioni randomizzate dell’Università di Aberdeen. Abbiamo utilizzato un algoritmo di minimizzazione che incorporava il centro, il rischio moderato o alto di TEV (il rischio di TEV non è stato incluso dopo il dicembre 2017 perché tutti i partecipanti reclutati dopo questa data erano ad alto rischio) e il sesso; è stato anche incorporato un elemento casuale. I partecipanti e gli investigatori non sono stati mascherati per l’assegnazione del trattamento. Gli scienziati o i tecnologi vascolari che hanno eseguito le ecografie duplex sono stati resi ciechi all’assegnazione dello studio. Ai partecipanti è stato chiesto di togliersi le calze e di non rivelare l’assegnazione del trattamento al personale che ha eseguito l’ecografia.
Interventi
Ai partecipanti di entrambi i gruppi di studio sono state somministrate dosi tromboprofilattiche di LMWH per il periodo di ricovero in ospedale. La formulazione di LMWH variava a seconda del centro, tuttavia il dosaggio era la dose tromboprofilattica standard del produttore per la formulazione. I partecipanti randomizzati a GCS adiuvante ricevuto sopra o sotto il ginocchio GCS (fornendo 18 mm di compressione Hg a livello della caviglia) oltre a LMWH. Ai partecipanti è stato chiesto di indossare GCS per la durata del ricovero in ospedale. La marca e la lunghezza della GCS fornita è stata guidata dalle politiche standard locali. Studi precedenti hanno dimostrato che la GCS sotto il ginocchio è paragonabile alla GCS a tutta lunghezza nella prevenzione della trombosi venosa profonda.13 Ai partecipanti randomizzati al solo LMWH è stato chiesto di non indossare alcun tipo di calza a compressione per 90 giorni dopo l’intervento.
Risultati
L’esito primario è stato un nuovo TEV entro 90 giorni dall’intervento chirurgico, sia trombosi venosa profonda degli arti inferiori con o senza sintomi, dimostrata da un’ecografia duplex, sia embolia polmonare con sintomi confermati dalla diagnostica per immagini. I partecipanti sono stati invitati a sottoporsi a un’ecografia bilaterale bilaterale completa dell’arto inferiore a due ecografie duplex tra i 14 e i 21 giorni dopo l’intervento chirurgico per rilevare il picco di incidenza di TEV.1415Sono state eseguite ecografie venose dell’intera gamba, che hanno valutato le vene profonde dalla vena femorale comune alle vene del polpaccio. I sintomi suggestivi di TEV potrebbero scatenare l’imaging in qualsiasi momento durante lo studio. In caso di diagnosi positiva, il team clinico e lo sperimentatore principale locale sono stati informati e il paziente è stato trattato secondo le linee guida dell’ospedale locale. Una copia anonima del rapporto di scansione è stata inviata al centro di coordinamento dello studio, dove l’esito primario è stato verificato da un esperto clinico indipendente in cieco. L’endpoint di 90 giorni è in linea con la definizione di trombosi acquisita in ospedale.161718Le misure di esito secondario comprendevano la qualità della vita (valutata utilizzando EQ-5D-5L (EuroQol cinque dimensioni cinque livelli)), la conformità con le calze e l’LMWH, le complicanze degli arti inferiori legate alla GCS, le complicanze emorragiche, le reazioni avverse all’LMWH e tutte cause di mortalità.
Analisi statistica
Il materiale supplementare fornisce tutti i dettagli dei calcoli originali e dei calcoli delle dimensioni del campione rivisti. La dimensione del campione originale era di 2236 per l’esito primario del TEV a 90 giorni. Questo campione doveva avere una potenza del 90% ad un livello di significatività del 2,5% per rilevare un margine di non inferiorità del 3,5% (considerato clinicamente importante) su un tasso di evento ipotizzato del 6% nel gruppo randomizzato a LMWH e GCS; questo tasso è stato corretto per una perdita del 10% per il follow-up e il disegno sequenziale del gruppo. Abbiamo derivato l’imaging ha confermato un tasso di eventi di TEV del 6% da una recente revisione sistematica che ha identificato studi randomizzati controllati con bracci che esplorano i risultati di TEV in pazienti che hanno subito un intervento chirurgico elettivo.10 Questo margine è stato scelto perché i medici non avrebbero tollerato un deterioramento assoluto del tasso di eventi TEV superiore al 3,5% rispetto alla terapia combinata. Il margine conserva anche il 61% dell’effetto terapeutico stabilito rispetto a nessun intervento. Quando abbiamo stratificato i pazienti in base all’età (<65 o ≥65 anni) e alla categoria di rischio di TEV (rischio moderato o alto), sono state identificate quattro sottopopolazioni.
Le analisi formali provvisorie nel disegno sequenziale di gruppo sono state specificate nel tempo dell’evento; cioè dopo che si erano accumulati diversi eventi. Dopo che il comitato direttivo di prova ha individuato un tasso di eventi complessivamente inferiore al previsto, il comitato indipendente di monitoraggio dei dati non è stato in grado di effettuare la prima analisi pianificata. Lo statistico senior in cieco ha invece eseguito un’analisi in cieco dei primi 1294 pazienti randomizzati, che ha identificato un gruppo in cui il tasso di eventi era più alto. Abbiamo ricalcolato le dimensioni del campione per quattro sottopopolazioni stratificate per età e rischio di TEV, abbandonando il disegno sequenziale del gruppo. Ad esempio, nel gruppo di pazienti di 65 anni e più, che sono stati valutati ad alto rischio di TEV, abbiamo avuto bisogno di 912 partecipanti, il che avrebbe permesso di rilevare un margine di non inferiorità del 4,0% assumendo un tasso di controllo del 3,6%.
Abbiamo analizzato il rischio di TEV entro 90 giorni dall’intervento chirurgico mediante una modellazione lineare generalizzata adattata al sesso e abbiamo aggiunto un errore di cluster robusto per il centro. Sono state eseguite sia l’intenzione di trattare che le analisi per protocollo, che includevano solo i partecipanti che hanno ricevuto l’intervento al quale sono stati randomizzati. Abbiamo utilizzato il limite superiore dell’intervallo di confidenza del 95% per la differenza di rischio per dedurre la non inferiorità. È stato calcolato un valore P di non inferiorità. Abbiamo eseguito analisi di sensibilità includendo solo i partecipanti che avevano una scansione duplex e separatamente includendo le esclusioni post-randomizzazione. Analisi simili sono state eseguite per le quattro sottopopolazioni, a meno che non esistesse un tasso di eventi pari a zero in ogni braccio, quando è stato riportato un intervallo di confidenza di incidenza assoluta unilaterale.
I dati dell’EQ-5D-5L sono stati analizzati utilizzando un modello di misure ripetute ad effetti misti regolato per il punteggio di base, il rischio di TEV, il sesso e un effetto casuale per il centro. Abbiamo eseguito limiti non parametrici19 per l’effetto causale medio per la conformità con le calze e il LMWH. I partecipanti sono stati classificati come pienamente conformi al LMWH se hanno ricevuto tutte le dosi di LMWH prescritte e parzialmente conformi quando hanno ricevuto più del 50% delle dosi prescritte. La conformità alla GCS è stata definita buona se i partecipanti hanno indossato le calze per almeno il 75% del ricovero ospedaliero. A causa del basso numero di eventi, non sono state previste analisi formali per le complicanze legate al GCS, le reazioni avverse al LMWH, le complicanze emorragiche e tutte causano mortalità. Le sottopopolazioni sono state analizzate in modo simile.
Abbiamo eseguito un’analisi post hoc del punteggio di Caprini per la popolazione di prova complessiva utilizzando un modello lineare generalizzato che si è adattato al sesso e abbiamo aggiunto un errore di cluster robusto per il centro. Per la nostra analisi, il punteggio di Caprini è stato classificato come basso-alto (punteggio <5) e più alto (punteggio ≥5) a causa del numero ridotto di partecipanti in alcune delle categorie. Abbiamo escluso i partecipanti da tutte le analisi se non si sono sottoposti a interventi chirurgici. Tutte le analisi sono state eseguite in versione Stata 15.20
Coinvolgimento del paziente e del pubblico
Un membro dell’ente di beneficenza registrato Thrombosis UK ha agito come rappresentante dei pazienti, assistendo dalle fasi di scrittura della borsa di studio fino al completamento dello studio. Ha anche fatto parte del comitato direttivo della sperimentazione, che ha preso tutte le decisioni principali, dalla pianificazione e progettazione, all’approvazione delle modifiche allo studio, all’assistenza nella diffusione dei risultati dello studio ai partecipanti allo studio e al pubblico in generale.
Risultati
Screening
Degli 11-679 partecipanti esaminati, 1905 sono stati randomizzati con 17 classificati con esclusioni post randomizzazione (fig. 1e tabella S2). Pertanto, sono stati inclusi 1888 partecipanti (948 nel solo gruppo LMWH e 940 nel gruppo LMWH e GCS). Di questi, 1858 hanno subito un intervento chirurgico (937 nel solo gruppo di LMWH e 921 nel gruppo di LMWH e GCS) e sono stati inclusi nell’intenzione di trattare l’analisi. La tabella S3 presenta i dettagli dei partecipanti in ogni sottopopolazione e la tabella S1 fornisce le ragioni per cui i partecipanti non erano idonei o hanno rifiutato di partecipare.
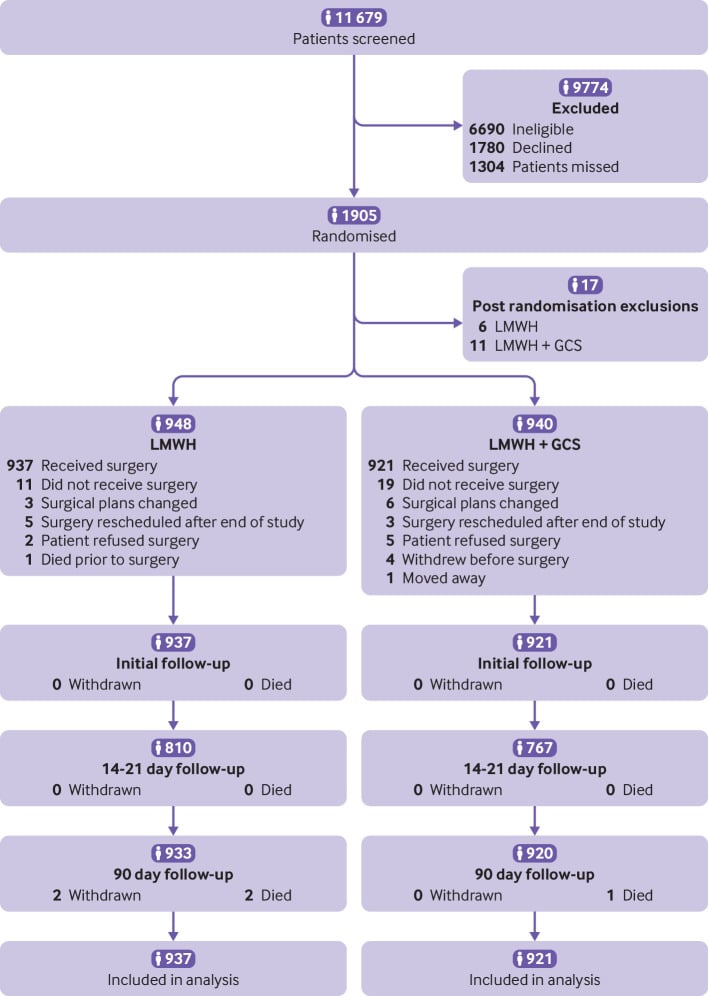
Fig. 1.Diagramma CONSORT (Consolidated Standards of Reporting Trials) che mostra la valutazione dell’idoneità, l’iscrizione e il follow-up
Le caratteristiche di base erano simili in entrambi i gruppi(tabella 1 e tabella S4) e nelle quattro sottopopolazioni (tabella S5). La chirurgia elettiva è stata eseguita in 937/948 (98,8%) partecipanti randomizzati al solo LMWH e 921/940 (98,0%) randomizzati al LMWH e al GCS (tabella S6). Le procedure chirurgiche più comuni erano generali (gastrointestinale superiore), ostetricia e ginecologia, e generali (gastrointestinale inferiore; tabella S6). L’intervento assegnato è stato eseguito in 758/948 (80,0%) nel solo gruppo LMWH e 750/940 (79,8%) nel gruppo LMWH e GCS (tabelle S6 e S7). Nel gruppo LMWH e GCS, 892/940 (94,9%) hanno ricevuto GCS, di cui 854/892 (95,7%) erano sotto il ginocchio (tabelle S6 e S7).
| Caratteristica | LMWH (n=948) | LMWH+GCS (n=940) |
|---|---|---|
| Età (anni) (media (SD)) | 59.3 (15.2) | 58.1 (14.9) |
| Sesso | ||
| Maschio | 347 (36.6) | 346 (36.8) |
| Femminile | 601 (63.4) | 594 (63.2) |
| Indice di massa corporea (media (SD)) | 28.7 (5.9) | 29.0 (6.1) |
| Rischio VTE | ||
| Moderato (punteggio 1) | 151 (15.9) | 150 (16.0) |
| Alto (punteggio ≥2) | 797 (84.1) | 790 (84.0) |
| Rischio di emorragia | ||
| Nessun rischio di sanguinamento | 918 (96.8) | 911 (96.9) |
| Uno o più fattori di rischio | 30 (3.2) | 29 (3.1) |
| Rischio Caprini | ||
| Basso (punteggio 0-1) | 4 (0.4) | 5 (0.5) |
| Moderato (punteggio 2) | 23 (2.4) | 28 (3.0) |
| Alto (punteggio 3-4) | 275 (29.0) | 267 (28.4) |
| Il più alto (punteggio ≥5) | 646 (68.1) | 640 (68.1) |
| EQ-5D-5L* (media (SD)) | 0.825 (0.185) | 0.817 (0.192) |
| EQ-5D VAS† (media (SD)) | 76.9 (17.5) | 77.0 (18.1) |
| Contraccettivi orali (solo donne) | ||
| Sì | 16/601 (2.7) | 24/594 (4.0) |
| No | 584/601 (97.2) | 570/594 (96.0) |
| Mancanza | 1/601 (0.2) | 0/594 (0) |
| Terapia ormonale sostitutiva (solo donne) | ||
| Sì | 35/601 (5.8) | 39/594 (6.6) |
| No | 565/601 (94.0) | 555/594 (93.4) |
| Mancanza | 1/601 (0.2) | 0/594 (0) |
| Storia della malignità | 213 (22.5) | 197 (21.0) |

Fig. 1.Diagramma CONSORT (Consolidated Standards of Reporting Trials) che mostra la valutazione dell’idoneità, l’iscrizione e il follow-up
Risultato primario
Nell’intenzione prestabilita di trattare l’analisi, il TEV si è verificato in 16/937 (1,7%) partecipanti nel solo gruppo LMWH rispetto a 13/921 (1,4%) nel gruppo LMWH e GCS (differenza di rischio 0,30%, intervallo di confidenza del 95% -0,65% a 1,26%; P<0,001 per non inferiorità; fig 2). Poiché l’intervallo di confidenza del 95% non ha superato il margine di non inferiorità del 3,5%, il gruppo randomizzato al solo LMWH si è dimostrato non inferiore. L’imaging ha confermato che l’embolia polmonare si è verificata in 2/937 (0,2%) partecipanti al solo gruppo LMWH rispetto a 1/921 (0,1%) nel gruppo LMWH e GCS. Trombosi venosa profonda con sintomi si è verificato in 2/937 (0,2%) partecipanti nel gruppo LMWH solo rispetto al 1/921 (0,1%) nel gruppo LMWH e GCS. Nei pazienti che hanno avuto pieno arti inferiori duplex imaging, trombosi venosa profonda senza sintomi è stato identificato in 12/810 (1,5%) i partecipanti nel gruppo LMWH solo rispetto al 11/767 (1,4%) nel gruppo LMWH e GCS(tabella 2).
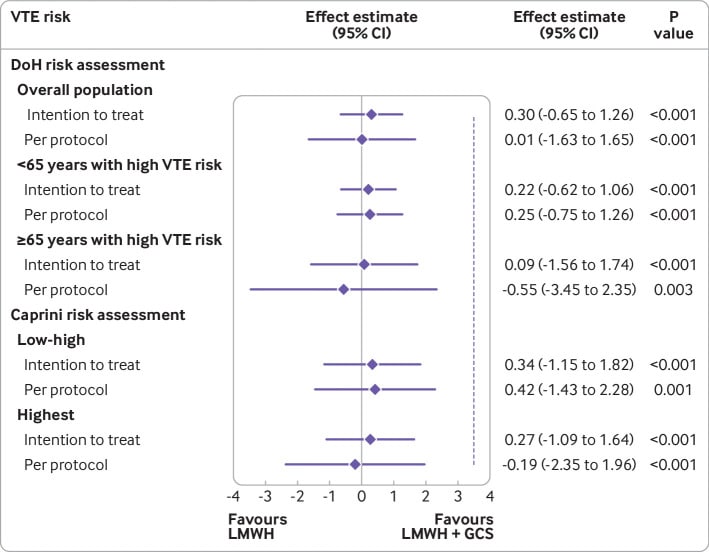
Fig 2.Fig. 2. Tromboembolia venosa (TEV) per la popolazione complessiva e le sottopopolazioni ad alto rischio di TEV (strumento di valutazione del rischio del Dipartimento della Salute (DoH)5) e per tutte le popolazioni (valutazione del rischio TEV Caprini7). I dati sono stime di effetto in percentuale. La linea verticale tratteggiata è il margine di non inferiorità (3,5%). GCS= calze a compressione graduata; LMWH= eparina a basso peso molecolare
| Tipo di VTE | LMWH | LMWH+GCS |
|---|---|---|
| Popolazione complessiva (LMWH n=937, LMWH+GCSn=921) | ||
| VTE entro 90 giorni | 16 (1.7) | 13 (1.4) |
| Tipo di VTE | ||
| TVDVT con sintomi | 2 (12.5) | 1 (7.7) |
| TVDVT senza sintomi identificati da duplex | 12 (75.0) | 11 (84.6) |
| L’imaging ha confermato un’embolia polmonare con sintomi | 2 (12.5) | 1 (7.7) |
| Comprese le esclusioni dopo la randomizzazione (LMWH n=943, LMWH+GCSn=932) | ||
| VTE entro 90 giorni | 16 (1.7) | 13 (1.4) |
| Tipo di VTE | ||
| TVDVT con sintomi | 2 (12.5) | 1 (7.7) |
| TVDVT senza sintomi identificati da duplex | 12 (75.0) | 11 (84.6) |
| L’imaging ha confermato un’embolia polmonare con sintomi | 2 (12.5) | 1 (7.7) |
| Inclusi i pazienti che hanno avuto una scansione duplex (LMWH n=810, LMWH+GCSn=767) | ||
| VTE entro 90 giorni | 16 (2.0) | 13 (1.7) |
| Tipo di VTE | ||
| TVDVT con sintomi | 2 (12.5) | 1 (7.7) |
| TVDVT senza sintomi identificati da duplex | 12 (75.0) | 11 (84.6) |
| L’imaging ha confermato un’embolia polmonare con sintomi | 2 (12.5) | 1 (7.7) |
| <65 anni con alto rischio di TAV (LMWH n=360, LMWH+GCSn=395) | ||
| VTE entro 90 giorni | 2 (0.6) | 1 (0.3) |
| Tipo di VTE | ||
| TVDVT con sintomi | 0 (0) | 1 (100.0) |
| DVT senza sintomi identificati da duplex | 2 (100.0) | 0 |
I risultati sono stati simili nell’analisi per protocollo (solo LMWH 12/758 (1,6%), LMWH e GCS 12/750 (1,6%); fig 2) e nell’analisi di sensibilità (tabella S8). La non inferiorità per il solo LMWH è stata mostrata in tutte le sottopopolazioni(fig 2 e tabella S9).

Fig 2.Tromboembolia venosa (TEV) per la popolazione complessiva e le sottopopolazioni ad alto rischio di TEV (strumento di valutazione del rischio del Dipartimento della Salute (DoH)5) e per tutte le popolazioni (valutazione del rischio di TEV di Caprini7). I dati sono stime di effetto in percentuale. La linea verticale tratteggiata è il margine di non inferiorità (3,5%). GCS= calze a compressione graduata; LMWH= eparina a basso peso molecolare
Risultati secondari
Non abbiamo trovato differenze nella qualità della vita tra i gruppi al punto di partenza, a una settimana o alla dimissione dall’ospedale, a 14-21 giorni o a 90 giorni(tabella 3). Complessivamente 750/940 (79,8%) partecipanti randomizzati a LMWH e GCS hanno avuto una buona conformità con le calze(tabella 3). La piena conformità al LMWH è stata raggiunta in 768/948 (81,0%) nel solo gruppo LMWH e in 755/940 (80,3%) nel gruppo LMWH e GCS (tabella 3).
| Qualità della vita e conformità | LMWH (n=948) | LMWH+GCS (n=940) | Differenza media (95% CI)† | Valore P |
|---|---|---|---|---|
| Chirurgia ricevuta (LMWH n=937, LMWH+GCSn=921) | ||||
| EQ-5D-5L (No; media (SD)) | ||||
| Base | 933; 0.825 (0.185) | 910; 0.818 (0.192) | — | — |
| 1 settimana o congedo | 874; 0.648 (0.232) | 839; 0.627 (0.244) | 0,015 (da -0,004 a 0,033) | 0.12 |
| 14-21 giorni | 846; 0.788 (0.202) | 820; 0.773 (0.206) | 0,011 (da -0,008 a 0,030) | 0.25 |
| 90 giorni | 774; 0.856 (0.192) | 743; 0.843 (0.197) | 0,011 (da -0,009 a 0,031) | 0.27 |
| EQ-5D VAS (No; media (SD)) | ||||
| Base | 932; 77.0 (17.4) | 907; 77.0 (18.2) | — | — |
| 1 settimana o di congedo | 873; 68.2 (19.5) | 837; 67.8 (20.1) | 0,23 (da -1,32 a 1,79) | 0.77 |
| 14-21 giorni | 846; 77.4 (17.4) | 819; 77.2 (17.0) | -0,04 (da -1,62 a 1,54) | 0.96 |
| 90 giorni | 773; 80.2 (17.9) | 743; 80.7 (18.2) | -0,29 (da -1,94 a 1,37) | 0.73 |
| Conformità al GCS* (No (%)) | 37 (4.0) | 750 (81.4) | (da -0,04 a 0,18) | — |
| Conformità con LMWH (No (%)) | ||||
| Ricevuto tutte le dosi di LMWH prescritte | 768 (82.0) | 755 (82.0) | (da -0,81 a 0,19) | — |
| Ricevuto ≥50% delle dosi prescritte | 779 (83.1) | 762 (82.7) | (da -0,82 a 0,18) | — |
Latabella 4 riassume le complicazioni e tutte causano la mortalità in base al trattamento ricevuto. Complicanze correlate alla GCS sono state segnalate in 50/787 (6,4%) pazienti che hanno ricevuto LMWH e GCS, e in 5/160 (3,1%) pazienti che hanno ricevuto solo GCS; la maggior parte di queste complicanze erano disturbi. Reazioni avverse al LMWH sono state segnalate in 6/779 (0,8%) pazienti che hanno ricevuto il solo LMWH e in 2/787 (0,3%) pazienti che hanno ricevuto LMWH e GCS(tabella 4). Due (0,3%) decessi si sono verificati in pazienti che hanno ricevuto il LMWH da solo e in 1/132 (0,8%) pazienti che non hanno ricevuto alcun trattamento; tutti i decessi non erano correlati né al LMWH né alla GCS. Sono stati segnalati eventi avversi gravi (n=239) in 210 partecipanti; otto eventi sono stati considerati probabilmente correlati al LMWH(tabella 4 e tabella S10).
| Complicazioni e mortalità | LMWH (n=779) | LMWH+GCS (n=787) | Solo GCS (n=160) | Nessuno dei due (n=132) |
|---|---|---|---|---|
| Complicazioni legate alla GCS* | 2 (0.3)† | 50 (6.4) | 5 (3.1) | 1 (0.8)† |
| Disagio | 2 | 41 | 4 | 1 |
| Rottura della pelle o ulcera | 0 | 1 | 0 | 0 |
| Eruzione cutanea | 0 | 4 | 0 | 0 |
| Altro | 0 | 21 | 1 | 0 |
| Reazioni avverse al LMWH* | 6 (0.8) | 2 (0.3) | 0 | 0 |
| Enzima epatico anormale | 7 | 0 | 0 | 0 |
| Altro | 2 | 2 | 0 | 0 |
| Complicazioni di sanguinamento | 5 (0.6) | 4 (0.5) | 1 (0.6) | 0 |
| Tutti causano mortalità | 2 (0.3) | 0 | 0 | 1 (0.8) |
Quando abbiamo utilizzato il punteggio Caprini al posto della valutazione del rischio di TEV del Dipartimento della Salute in un’analisi post hoc, 1286/1888 (68,1%) partecipanti sono stati classificati a più alto rischio di TEV (punteggio ≥5). Per i pazienti che hanno subito un intervento chirurgico, si sono verificati 14/640 (2,2%) episodi di TEV nel solo gruppo LMWH rispetto a 12/625 (1,9%) nel gruppo LMWH e GCS (differenza di rischio 0,27%, intervallo di confidenza del 95% da -1,09% a 1,64%, P<0,001 per non inferiorità) (fig. 2e tabella S11).
Discussione
Principali risultati
Questo studio randomizzato multicentrico e pragmatico ha dimostrato che la farmaco-tromboprofilassi con il solo LMWH non è inferiore alla farmaco-tromboprofilassi con LMWH e GCS in pazienti che hanno subito un intervento chirurgico elettivo e sono stati valutati a rischio moderato o elevato di TEV. Questo risultato è stato sostenuto quando abbiamo esaminato le sottopopolazioni in base all’età (<65 o ≥65 anni) e al rischio di TEV di base (moderato o alto).
Punti di forza e di debolezza dello studio
La casistica delle procedure chirurgiche elettive incluse in questo studio è simile alle proporzioni intraprese a livello nazionale nel Regno Unito. Pertanto, i risultati sembrano essere applicabili alla più ampia popolazione chirurgica elettiva. La maggior parte dei partecipanti a questo studio è stata considerata nella categoria di rischio più elevato per il TEV, sia che sia stata valutata utilizzando lo strumento di valutazione del rischio del Dipartimento della Salute5 o il punteggio Caprini.7
Riconosciamo che il nostro studio ha dei limiti. In primo luogo, 281/1858 (15,1%) dei partecipanti non hanno ricevuto un’ecografia duplex, che avrebbe potuto rilevare più pazienti con trombosi venosa profonda senza sintomi. Tuttavia, la proporzione era relativamente piccola e il numero di ecografie mancanti è stato distribuito in modo comparabile tra i due gruppi randomizzati. La proporzione che non ha ricevuto un’ecografia duplex avrebbe dovuto contribuire all’incirca a un evento asintomatico aggiuntivo per ogni gruppo di trattamento, e quindi probabilmente non avrebbe influenzato i risultati complessivi. In secondo luogo, il sottogruppo di partecipanti di età pari o superiore ai 65 anni valutati come a moderato rischio di TEV era sottorappresentato nello studio, il che riflette il fatto che questo gruppo è sottorappresentato nella popolazione generale. Infatti, 797/948 (84,1%) partecipanti nel solo gruppo LMWH e 790/940 (84,0%) nel gruppo LMWH e GCS sono stati valutati come ad alto rischio (punteggio ≥2) di TEV secondo lo strumento di valutazione del rischio di TEV del Dipartimento della Salute. Inoltre, più di due terzi dei partecipanti sono risultati a rischio più elevato (punteggio ≥5) se valutati utilizzando il punteggio Caprini, con una non inferiorità del solo LMWH rispetto al LMWH e al GCS in queste popolazioni a rischio più elevato.
Confronto con altri studi
I risultati del nostro studio si aggiungono ad un numero crescente di prove che non supportano l’uso della GCS quando le misure farmacologiche non sono controindicate e vengono fornite.821Nella popolazione del nostro studio, 854/892 (95,7%) partecipanti hanno ricevuto sotto le calze da ginnastica, il che probabilmente riflette la pratica del Regno Unito. Questo studio non può assolutamente concludere che la GCS per la lunghezza delle cosce non abbia alcun beneficio. Tuttavia, in uno studio randomizzato controllato di pazienti ricoverati con ictus acuto, la lunghezza delle cosce GCS non ha ridotto significativamente il rischio di sviluppare trombosi venosa profonda femoro-poplitea con o senza sintomi,9 e sono stati associati con più complicazioni cutanee. Questi risultati hanno portato ad una riduzione dell’uso della GCS nei pazienti con ictus.
I risultati di questo studio sono supportati da dati provenienti da un unico centro in cui la politica è stata quella di non utilizzare la GCS nei pazienti sottoposti a chirurgia elettiva a cui viene somministrata una dose tromboprofilattica di LMWH. I risultati di TEV riportati da questo centro sono paragonabili ai dati nazionali.22
Significato dello studio
Una riduzione del 15,4% della mortalità per TEV a 90 giorni è stata recentemente riportata dopo l’introduzione di un approccio sistematico per la prevenzione del TEV associato all’ospedale nel Regno Unito nel 2010.23 Un’opinione afferma che “siamo entrati in un’era in cui i tassi di TEV dopo l’intervento chirurgico sono diminuiti in modo significativo grazie al miglioramento delle cure e alla farmacotromboprofilassi tale che la tromboprofilassi combinata con LMWH e GCS potrebbe non essere più necessaria” 23
È degno di nota il fatto che in questo studio i tassi di eventi sono stati molto più bassi del previsto sulla base di studi pubblicati in precedenza.10 Questi tassi potrebbero essere in parte attribuiti a periodi di permanenza più brevi, a migliori tecniche operative e a regimi analgesici che consentono una mobilizzazione anticipata. È chiaro che le attuali linee guida si basano in gran parte su dati storici e dovrebbero essere riviste.
I risultati di questo studio avranno probabilmente implicazioni cliniche sulla somministrazione di GCS in pazienti sottoposti a procedure chirurgiche elettive. Le stime iniziali del costo annuale per l’acquisto e l’applicazione della GCS ai pazienti chirurgici valutati a rischio moderato o elevato di TEV hanno superato i 63 milioni di sterline in Inghilterra (79 milioni di dollari; 72 milioni di euro).12 Una sostanziale riduzione di questi costi, scalata a livello globale e su base ricorrente, ha il potenziale per avere un importante impatto finanziario positivo sui sistemi sanitari ospedalieri.
In conclusione, questo studio multicentrico randomizzato ha dimostrato che il solo LMWH non è inferiore al LMWH e alla GCS per la prevenzione del TEV in pazienti sottoposti a chirurgia elettiva che sono a moderato o alto rischio di TEV. La non inferiorità è stata dimostrata nelle singole sottopopolazioni a rischio. Se si considerano i potenziali eventi avversi e il costo della GCS, si raccomanda una revisione urgente delle linee guida nazionali e internazionali per la prevenzione del TEV.
Domande senza risposta e ricerche future
Abbiamo escluso i pazienti in cui le prove attuali supportano la profilassi farmacologica dei TEV dopo la dimissione dall’ospedale,124 come quelli sottoposti a chirurgia sostitutiva delle articolazioni o a resezioni di tumore addominopelvico. Questa esclusione dovrebbe essere presa in considerazione nella traduzione e nell’implementazione dei risultati di questo studio nella pratica clinica. Sono necessari ulteriori studi per valutare il beneficio adiuvante della GCS in questi gruppi di pazienti e in quelli sottoposti a interventi chirurgici in situazioni di emergenza.
Ciò che è già noto su questo argomento
- La profilassi del tromboembolismo venoso è necessaria nella maggior parte dei pazienti sottoposti a procedure chirurgiche
- Il beneficio coadiuvante delle calze a compressione graduata oltre alla farmacotromboprofilassi in questi pazienti non è chiaro
Cosa aggiunge questo studio
- Questo studio ha dimostrato che nei pazienti che hanno subito interventi chirurgici elettivi e sono stati valutati a rischio moderato o elevato di tromboembolismo venoso, la sola farmacotromboprofilassi non è inferiore alla farmacotromboprofilassi e alle calze a compressione graduata.
- Le attuali linee guida basate su dati storici dovrebbero essere riviste
References
- Publisher Full Text
- Sachdeva A, Dalton M, Lees T. Graduated compression stockings for prevention of deep vein thrombosis. Cochrane Database Syst Rev. 2018; 11DOI | PubMed
- Xu K, Chan NC, Ibrahim Q. Reduction in mortality following elective major hip and knee surgery: a systematic review and meta-analysis. Thromb Haemost. 2019; 119:668-74. DOI | PubMed
- Mismetti P, Laporte S, Darmon JY, Buchmüller A, Decousus H. Meta-analysis of low molecular weight heparin in the prevention of venous thromboembolism in general surgery. Br J Surg. 2001; 88:913-30. DOI | PubMed
- Publisher Full Text
- Gould MK, Garcia DA, Wren SM. Prevention of VTE in nonorthopaedic surgical patients: antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012; 141(Suppl):e227S-77S. DOI | PubMed
- Caprini JA. Thrombosis risk assessment as a guide to quality patient care. Dis Mon. 2005; 51:70-8. DOI | PubMed
- Whittaker L, Baglin T, Vuylsteke A. Challenging the evidence for graduated compression stockings. BMJ. 2013; 346:f3653. DOI | PubMed
- Dennis M, Sandercock PA, Reid J, CLOTS Trials Collaboration. Effectiveness of thigh-length graduated compression stockings to reduce the risk of deep vein thrombosis after stroke (CLOTS trial 1): a multicentre, randomised controlled trial. Lancet. 2009; 373:1958-65. DOI | PubMed
- Mandavia R, Shalhoub J, Head K, Davies AH. The additional benefit of graduated compression stockings to pharmacologic thromboprophylaxis in the prevention of venous thromboembolism in surgical inpatients. J Vasc Surg Venous Lymphat Disord. 2015; 3:447-455.e1. DOI | PubMed
- Cohen AT, Skinner JA, Warwick D, Brenkel I. The use of graduated compression stockings in association with fondaparinux in surgery of the hip. A multicentre, multinational, randomised, open-label, parallel-group comparative study. J Bone Joint Surg Br. 2007; 89:887-92. DOI | PubMed
- Shalhoub J, Norrie J, Baker C, GAPS Trial Investigators. Graduated compression stockings as an adjunct to low dose low molecular weight heparin in venous thromboembolism prevention in surgery: a multicentre randomised controlled trial. Eur J Vasc Endovasc Surg. 2017; 53:880-5. DOI | PubMed
- Sajid MS, Tai NR, Goli G, Morris RW, Baker DM, Hamilton G. Knee versus thigh length graduated compression stockings for prevention of deep venous thrombosis: a systematic review. Eur J Vasc Endovasc Surg. 2006; 32:730-6. DOI | PubMed
- Sweetland S, Green J, Liu B, Million Women Study collaborators. Duration and magnitude of the postoperative risk of venous thromboembolism in middle aged women: prospective cohort study. BMJ. 2009; 339:b4583. DOI | PubMed
- Warwick D, Rosencher N. The “critical thrombosis period” in major orthopedic surgery: when to start and when to stop prophylaxis. Clin Appl Thromb Hemost. 2010; 16:394-405. DOI | PubMed
- Khan DMI, Leary C, Hayes MA. Current practice of hospital acquired thrombosis (HAT) prevention in an acute hospital (a single centre cross sectional study). Blood. 2015; 126:4459. DOI
- Litchfield I, Fitzmaurice D, Apenteng P. Prevention of hospital-acquired thrombosis from a primary care perspective: a qualitative study. Br J Gen Pract. 2016; 66:e593-602. DOI | PubMed
- Khan MI, O’Leary C, O’Brien A. Hospital acquired thrombosis (HAT) prevention in an acute hospital; a single centre cross-sectional study. Ir Med J. 2017; 110:547. PubMed
- Palmer TM, Ramsahai RR, Didelez V, Sheehan NA. Nonparametric bounds for the causal effect in a binary instrumental-variable model. Stata J. 2011; 11:345-67. DOI
- StataCorp. Stata Statistical Software.. StataCorp; 2017.
- Welfare M. NICE’s recommendations for thromboembolism are not evidence based. BMJ. 2011; 343:d6452. DOI | PubMed
- McQuaid N, Davies P, Everington T. Updated 2018 NICE guidance on venous thromboembolism – does evidence from root cause analysis of hospital-associated thrombosis support the additional investment required?. Br J Haematol. 2019; 185:773-5. DOI | PubMed
- Hunt BJ. Preventing hospital associated venous thromboembolism. BMJ. 2019; 365:l4239. DOI | PubMed
- Guyatt GH, Norris SL, Schulman S. Methodology for the development of antithrombotic therapy and prevention of thrombosis guidelines: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012; 141(Suppl):53S-70S. DOI | PubMed
Fonte
Shalhoub J, Lawton R, Hudson J, Baker C, Bradbury A, et al. (2020) Graduated compression stockings as adjuvant to pharmaco-thromboprophylaxis in elective surgical patients (GAPS study): randomised controlled trial. The BMJ 369m1309. https://doi.org/10.1136/bmj.m1309





