Abstract
Introduzione
Negli Stati Uniti, il diabete è la principale causa di malattia renale allo stadio terminale (ESRD), che è l’insufficienza renale trattata con la dialisi o il trapianto (1). La prevalenza del diabete tra gli indiani d’America e gli Alaska Natives (AI/AN) negli Stati Uniti nel 2012 (15,9%) è stata superiore a quella dei neri non ispanici (neri) (13,2%), degli ispanici (12,8%) o dei bianchi non ispanici (bianchi) (7,6%) nel periodo 2010-2012 (2). Il diabete rappresenta il 44% dei nuovi casi di ESRD (ESRD-associati al diabete [ESRD-D]) nella popolazione statunitense complessiva e il 69% tra gli AI/AN (1). La prevenzione o il ritardo dell’ESRD-D comporta il controllo della pressione sanguigna e del glucosio nel sangue, l’identificazione precoce e il monitoraggio delle malattie renali e l’uso di inibitori dell’enzima di conversione dell’angiotensina (ACE) e di bloccanti del recettore dell’angiotensina II (ARB) nei pazienti con albuminuria (3,4). Questo rapporto presenta le tendenze nell’incidenza dell’ESRD-D per l’AI/AN rispetto ad altri gruppi razziali/etnici, e discute i probabili fattori che hanno influenzato i miglioramenti osservati in questa popolazione durante il periodo 1996-2013.
Metodi
Medicare copre il trattamento ESRD per i beneficiari indipendentemente dall’età e paga la maggior parte del costo del trattamento ESRD negli Stati Uniti (1). L’U.S. Renal Data System (USRDS) è un sistema di sorveglianza per l’ESRD basato sui rapporti dei dati clinici e sui dati dei sinistri ai Centers for Medicare & Medicaid Services (CMS). Finanziato dal National Institute of Diabetes and Digestive and Kidney Diseases dei National Institutes of Health, l’USRDS raccoglie, analizza e distribuisce dati demografici e clinici sui pazienti in trattamento per l’ESRD, compresa la diagnosi primaria o la causa dell’insufficienza renale. Poiché la maggior parte dei pazienti ESRD diventano idonei alla copertura Medicare dopo 90 giorni di trattamento ESRD, solo i dati sui pazienti che sono stati trattati per almeno 90 giorni sono inclusi nel set di dati (1).
Per ogni anno studiato, i dati USRDS sono stati utilizzati per determinare il numero di adulti di età ≥18 anni negli Stati Uniti che hanno iniziato il trattamento (dialisi o trapianto di rene) per l’ESRD-D. I dati sono stati analizzati per i gruppi razziali AI/AN, bianchi, neri e asiatici, che includono persone di origine ispanica e non ispanica. I dati per le persone di origine ispanica sono stati analizzati separatamente.
L’incidenza ESRD-D è stata calcolata utilizzando il numero di casi ESRD-D appena trattati e due stime della popolazione per ogni gruppo razziale ed etnico: 1) la popolazione totale del censimento statunitense nel periodo 1996-2013 e 2) la popolazione con diabete diagnosticato nel periodo 2006-2013.
Il numero di AI/AN con diabete diagnosticato è stato calcolato utilizzando le stime di prevalenza specifiche per età e sesso del National Data Warehouse del Servizio sanitario indiano (IHS) nel corso del 2006-2013 e moltiplicandole per le stime annuali della popolazione di una singola razza per l’AI/AN del censimento statunitense; il 2006 è stato il primo anno per il quale sono disponibili dati di prevalenza coerenti. Il National Data Warehouse dell’IHS comprende la registrazione dei pazienti e i dati relativi alle strutture IHS, ai programmi sanitari gestiti a livello tribale e ai sistemi sanitari urbani indiani (I/T/U). * Queste strutture servono circa 2,2 milioni di persone AI/AN che appartengono a 567 tribù riconosciute a livello federale in 36 stati.† I casi di diabete sono stati identificati utilizzando i codici diagnostici 250.0-250.93 della Classificazione Internazionale delle Malattie, Nona revisione, Modifica Clinica. Si è ritenuto che i pazienti abbiano diagnosticato il diabete se hanno avuto almeno due visite sanitarie con un codice di diagnosi di diabete riportato durante l’anno fiscale (5). Per gli altri gruppi razziali ed etnici, le stime della popolazione adulta con diabete diagnosticato (autodenunciato) sono state ricavate dal National Health Interview Survey.§
I tassi di incidenza ESRD-D sono stati corretti in base all’età sulla base della popolazione standard statunitense del 2000, e la regressione del joinpoint è stata utilizzata per analizzare le tendenze (6,7). Ogni segmento di tendenza è descritto da una variazione percentuale annua (APC) con un intervallo di confidenza del 95% (CI), e la tendenza per l’intero periodo di studio è descritta dalla variazione percentuale media annua (AAPC). Il tasso di variazione per le tendenze lineari è stato testato per determinare se era significativamente diverso da zero. I risultati sono stati considerati significativi se il valore p era <0,05.
Le misure di cura per l’AI/AN con diabete sono state ottenute dall’IHS Diabetes Care and Outcomes Audit (Audit), che comprende la prescrizione di ACE inibitori e ARB, la pressione sanguigna, l’emoglobina A1C per valutare il controllo del glucosio e il test del rapporto urina-albumina-creatinina per identificare e monitorare la malattia renale diabetica. L’Audit è un processo annuale per valutare la cura del diabete e gli esiti sanitari per l’AI/AN con diabete diagnosticato che riceve assistenza presso strutture I/T/U, tracciando le prestazioni su diverse decine di misure di cura del diabete e la prevalenza di diverse complicanze del diabete, tra cui la malattia renale.¶
Risultati
Tra gli adulti AI/AN, l’incidenza ESRD-D corretta per età per 100.000 persone è aumentata, ma non in modo significativo, da 57,3 nel 1996 a 63,5 nel 1999 per poi scendere a 26,5 nel 2013, con un calo del 54% (AAPC = -4,4% all’anno [95% CI = -5,7% a -3,0%], p<0,001) per tutto il periodo di studio (Figura 1) (Tabella 1). Tra gli altri gruppi razziali/etnici, l’incidenza del ESRD-D tra gli adulti aggiustata per età è diminuita a partire dal 1998 per gli asiatici, dal 2001 per i neri, dal 2006 per i bianchi e dal 2000 per gli ispanici.
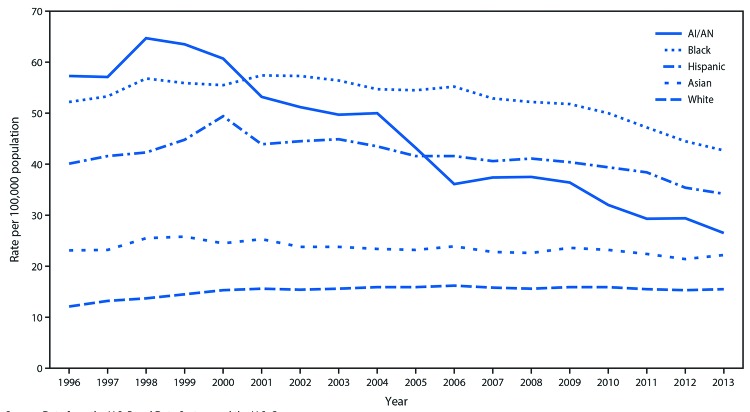
FIGURA 1.Incidenza* della malattia renale allo stadio finale del diabete tra gli adulti di età ≥18 anni, per razza ed etnia – Stati Uniti, 1996-2013Fonte: Dati provenienti dal Renal Data System degli Stati Uniti e dal Censimento degli Stati Uniti.Abbreviazione: AI/AN=Indiani americani e nativi dell’Alaska.* Tasso per 100.000 abitanti e per età, aggiustato in base alla popolazione standard statunitense del 2000. I gruppi razziali comprendono persone di origine ispanica e non ispanica; gli ispanici possono essere di qualsiasi razza.
| Popolazione generale | Vota | Variazione percentuale | Tendenza generale | Segmento di tendenza 1§ | Segmento di tendenza 2/3§ | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1996 | 2013 | AAPC (95% CI) | p valore | Periodo | APC (95% CI) | p valore | Periodo | APC (95% CI) | p valore | ||
| Popolazione diabetica | Vota | Variazione percentuale | Tendenza generale | Segmento di tendenza 1§ | Segmento di tendenza 2/3§ | ||||||
| 2006 | 2013 | AAPC (95% CI) | p valore | Periodo | APC (95% CI) | p valore | Periodo | APC (95% CI) | p valore | ||
| AI/AN | 57.3 | 26.5 | −54 | -4,4 (da -5,7 a -3,0) | <0.001 | 1996–1999 | 3,3 (da -4,7 a 12,0) | 0.40 | 1999–2013 | -6,0 (da -6,7 a -5,2) | <0.001 |
| Asiatici | 23.1 | 22.2 | −4 | -0,2 (da -1,0 a 0,6) | 0.62 | 1996–1998 | 5,4 (da -2,2 a 13,6) | 0.15 | 1998–2013 | -0,9 (da -1,2 a -0,6) | <0.001 |
| Neri | 52.2 | 42.7 | −18 | -1,3 (da -1,8 a -0,7) | <0.001 | 1996–2001 | 1,7 (da 0,5 a 2,9) | 0.01 | 2001–2009 | -1,3 (da -2,0 a -0,6) | 0.002 |
| 2009–2013 | -4,8 (da -6,4 a -3,2) | <0.001 | |||||||||
| Bianchi | 12.1 | 15.5 | +28 | 1,4 (da 0,9 a 1,8) | <0.001 | 1996–2000 | 5,8 (da 4,5 a 7,1) | <0.001 | 2000–2006 | 0,7 (da -0,1 a 1,6) | 0.09 |
| 2006–2013 | -0,6 (da -1,1 a -0,1) | 0.03 | |||||||||
| Ispanici | 40.1 | 34.2 | −15 | -0,6 (da -1,3 a 0,1) | 0.08 | 1996–2000 | 4,4 (da 1,6 a 7,3) | 0.005 | 2000–2013 | -2,1 (da -2,5 a -1,6) | <0.001 |
| AI/AN | 210.7 | 152.7 | −28 | -4,9 (da -7,0 a -2,7) | <0.001 | 2006–2009 | -2,0 (da -8,2 a 4,7) | 0.41 | 2009–2013 | -7,0 (da -10,8 a -3,0) | 0.01 |
| Asiatici | 219.0 | 227.4 | +4 | -0,8 (da -5,9 a 4,6) | 0.72 | 2006–2013 | -0,8¶(da -5,9 a 4,6) | 0.72 | — | — | — |
| Neri | 379.8 | 329.6 | −13 | -2,8 (-4,7 a -1,0) | 0.01 | 2006–2013 | -2,8¶(da -4,7 a -1,0) | 0.01 | — | — | — |
| Bianchi | 185.8 | 159.0 | −14 | -2,0 (da -3,9 a -0,0) | 0.05 | 2006–2013 | -2,0¶(da -3,9 a -0,0) | 0.05 | — | — | — |
| Ispanici | 287.6 | 223.0 | −22 | -0,1 (da -0,1 a -0,1) | <0.001 | 2006–2008 | -0,3 (da -0,5 a -0,1) | 0.01 | 2008–2013 | -0,0 (da -0,0 a 0,0) | 0.79 |
Tra gli adulti AI/AN con diabete, l’incidenza di ESRD-D è diminuita nel periodo 2009-2013 (APC = -7,0% all’anno [da -10,8% a -3,0%], p = 0,01) e, entro il 2013, è stata simile a quella dei bianchi con diabete (152,7 contro 159,0 per 100.000 diabetici, p = 0,84) (Figura 2) (Tabella 1). Tra gli altri gruppi razziali/etnici con diabete, l’incidenza del ESRD-D è diminuita nei neri e nei bianchi durante il periodo 2006-2013, e non ha mostrato una tendenza costante tra gli asiatici. Tra gli ispanici, ESRD-D incidenza è diminuita nel corso del 2006-2008, e poi livellato.
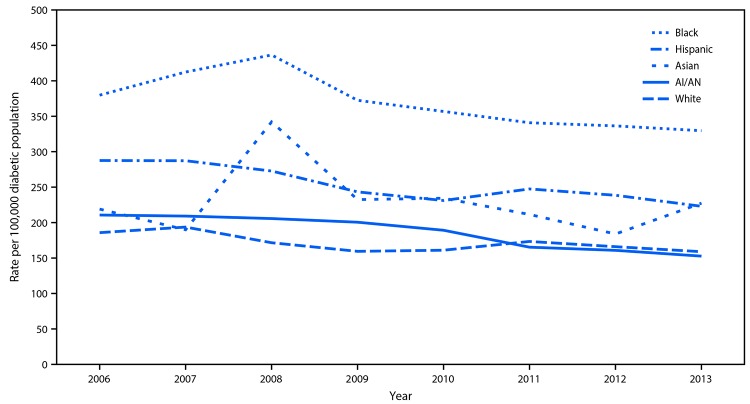
FIGURA 2.Incidenza* della malattia renale in stadio terminale correlata al diabete tra gli adulti di età ≥18 anni con diabete, per razza ed etnia – Stati Uniti, 2006-2013Fonti: U.S. Renal Data System, U.S. Diabetes Surveillance System, e dati del servizio sanitario indiano applicati alla popolazione del censimento statunitense.Abbreviazione: AI/AN=Indiani americani e nativi dell’Alaska.* Tasso per 100.000 persone diabetiche e per età adattato in base alla popolazione standard statunitense del 2000. I gruppi razziali comprendono persone di origine ispanica e non ispanica; gli ispanici possono essere di qualsiasi razza.
I dati dell’Audit mostrano che la prescrizione di ACE inibitori e ARB per i pazienti AI/AN con diabete è aumentata in modo sostanziale, dal 42% nel 1997 al 74% nel 2002, per poi rimanere stabile, dal 68% al 73% ogni anno fino al 2015(Figura 3). Tra i pazienti AI/AN con diabete e ipertensione o malattie renali croniche (CKD), la prescrizione di ACE inibitori e ARB è stata >77% per ogni anno studiato. Inoltre nel 2014, tra gli AI/AN con diabete, al 76% sono stati prescritti ACE inibitori o ARB, rispetto al 56% degli adulti con diabete nella popolazione generale degli Stati Uniti nel periodo 2009-2014, valutati utilizzando i dati del National Health and Nutrition Examination Survey (8).** I livelli medi di pressione sanguigna in AI/AN con diabete sono stati ben controllati dal 1997, il primo anno in cui tali dati erano disponibili. Nel 2015, la pressione sanguigna media tra >101.000 AI/AN nell’Audit con diabete e ipertensione era di 133/76 mmHg, al di sotto dell’obiettivo di <140/90.†† I livelli medi di emoglobina A1C nell’AI/AN con diabete sono diminuiti del 10% dal 1996 al 2014, passando dal 9,0% all’8,1% (9). Infine, il test del rapporto urina-albumina-creatinina è stato eseguito nel 50% dell’AI/AN di età ≥65 anni con diabete nel 2013, aumentando al 62% entro il 2016. Nella popolazione diabetica generale di Medicare di età ≥65 anni, il tasso di test dell’albumina urinaria è stato del 40% nel 2013 (1).
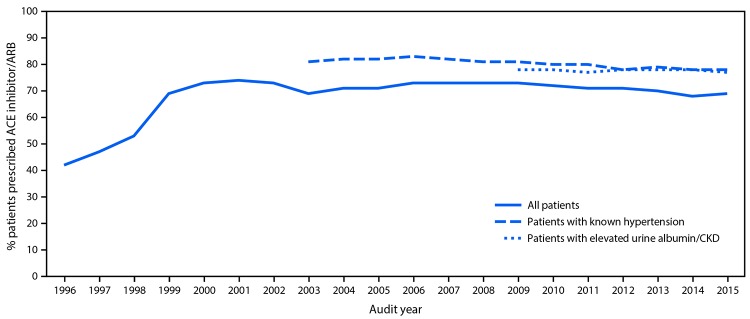
FIGURA 3.prescrizione di ACE Inhibitor/ARB in pazienti affetti da diabete, 1996-2015Fonte: Servizio sanitario indiano Diabetes Care and Outcomes Audit.Abbreviazioni: ACE = enzima di conversione dell’angiotensina; AI/AN = indiani d’America e nativi dell’Alaska; ARB = bloccante del recettore dell’angiotensina; CKD = malattia renale cronica.

FIGURA 1.Incidenza* della malattia renale in stadio terminale correlata al diabete tra gli adulti di età ≥18 anni, per razza ed etnia – Stati Uniti, 1996-2013Fonte: Dati provenienti dal Renal Data System degli Stati Uniti e dal Censimento degli Stati Uniti.Abbreviazione: AI/AN=Indiani americani e nativi dell’Alaska.* Tasso per 100.000 abitanti e per età, aggiustato in base alla popolazione standard statunitense del 2000. I gruppi razziali comprendono persone di origine ispanica e non ispanica; gli ispanici possono essere di qualsiasi razza.

FIGURA 2.Incidenza* della malattia renale allo stadio finale del diabete tra gli adulti di età ≥18 anni affetti da diabete, per razza ed etnia – Stati Uniti, 2006-2013Fonti: U.S. Renal Data System, U.S. Diabetes Surveillance System, e dati del servizio sanitario indiano applicati alla popolazione del censimento statunitense.Abbreviazione: AI/AN=Indiani americani e nativi dell’Alaska.* Tasso per 100.000 persone diabetiche e per età adattato in base alla popolazione standard statunitense del 2000. I gruppi razziali comprendono persone di origine ispanica e non ispanica; gli ispanici possono essere di qualsiasi razza.

FIGURA 3.ACE Inibitore/ARB prescrizione di ACE in pazienti affetti da AI/AN con diabete, 1996-2015Fonte: Servizio sanitario indiano Diabetes Care and Outcomes Audit.Abbreviazioni: ACE = enzima di conversione dell’angiotensina; AI/AN = indiani d’America e nativi dell’Alaska; ARB = bloccante del recettore dell’angiotensina; CKD = malattia renale cronica.
Conclusioni e commenti
Tra gli adulti affetti da AI/AN, l’incidenza dell’ESRD-D regolata in base all’età è diminuita del 54% nel periodo 1996-2013; nel 2013, tra gli adulti affetti da diabete, il tasso di ESRD-D è stato lo stesso per l’AI/AN che per i bianchi. Questo calo è particolarmente notevole se si considerano le ben documentate disparità sanitarie e socioeconomiche nella popolazione AI/AN, tra cui la povertà, le limitate risorse sanitarie e l’onere sproporzionato di molti problemi di salute (10). I risultati di questo rapporto sono coerenti con altri studi tra gli AI/AN a livello nazionale e tra gli indiani Pima nel sud-ovest, che hanno concluso che il miglioramento della pressione sanguigna, la glicemia e l’uso di ACE inibitori e ARB hanno giocato un ruolo significativo nel declino dell’ESRD-D in queste popolazioni (11,12).
La diminuzione dell’ESRD-D nell’AI/AN con diabete è stata probabilmente il risultato di miglioramenti sia nel processo che nelle misure di esito presentate in questo rapporto. La prescrizione di ACE inibitori e ARB nell’AI/AN con diabete è aumentata del 76% dal 1997 al 2002. Nel 2014, la prescrizione di questi farmaci tra gli AI/AN con diabete è stata superiore del 36% rispetto alla popolazione statunitense complessiva con diabete (8). Analogamente, tra le persone con diabete di età ≥65 anni, il tasso di test del rapporto urina-albumina-creatinina è del 55% più alto nell’AI/AN rispetto ai beneficiari di Medicare (1). Anche le misure di risultato sono positive, tra cui il controllo della pressione sanguigna in AI/AN con diabete e ipertensione e il miglioramento del controllo glicemico in generale. La definizione e il sostegno di queste tendenze favorevoli nella gestione del diabete e nella prevenzione dell’ESRD-D sono legate agli approcci alla gestione del diabete adottati dall’IHS da parte della popolazione e del team.
A partire dalla metà degli anni ’80, l’IHS ha implementato approcci sistematici alla cura del diabete che hanno contribuito ai risultati qui presentati (13,14). Questi approcci sono stati informati dai principi di salute pubblica e di gestione della popolazione, che si concentrano non solo sui risultati a breve termine per i singoli pazienti che cercano assistenza, ma anche sui risultati a lungo termine, i costi, le disparità e il benessere dell’intera comunità (15). Questi approcci includono l’assistenza e l’educazione clinica multidisciplinare basata su team multidisciplinari e coordinata, la sensibilizzazione della comunità e il monitoraggio dei dati relativi ai processi clinici e ai risultati a livello locale, regionale e nazionale (9).
Questo sistema IHS di cura del diabete ha permesso ai siti I/T/U di fornire con successo e in modo coerente interventi basati sull’evidenza che riducono i fattori di rischio ESRD-D. Nel 1986, IHS ha sviluppato il suo primo Diabetes Standards of Care per diffondere le raccomandazioni basate sulle evidenze per migliorare la cura del diabete per l’AI/AN (13). Questi standard sono stati rivisti all’inizio degli anni ’90 per includere la valutazione e il trattamento della CKD (16). IHS è stato uno dei primi sistemi a stabilire la segnalazione di routine del tasso di filtrazione glomerulare stimato, il monitoraggio annuale dell’escrezione di albumina urinaria e la prescrizione di ACE inibitori e ARB (14). Entrambe queste classi di agenti terapeutici hanno dimostrato di prevenire o ritardare lo sviluppo di ESRD-D nei pazienti con albuminuria, indipendentemente dai loro effetti nella riduzione della pressione sanguigna (4,17).
Poiché la raccolta e l’analisi dei dati sono componenti fondamentali di un efficace sistema di cura del diabete, IHS ha implementato per la prima volta l’Audit Diabetes Care and Outcomes nel 1986 in diversi siti e nel 1997 ha sviluppato un database nazionale centralizzato (18). Il successo dell’implementazione di interventi clinici basati sull’evidenza, come documentato dall’Audit, potrebbe spiegare in parte la diminuzione dell’incidenza dell’ESRD-D negli adulti affetti da diabete. L’IHS ha apportato altri miglioramenti nella cura del diabete sviluppando programmi e strumenti di educazione clinica, materiali di educazione dei pazienti culturalmente rilevanti e strumenti di gestione basati sulla popolazione nella cartella clinica elettronica dell’IHS (9,14,19). I case manager I/T/U aiutano a coordinare l’assistenza interna e le referenze per i servizi specializzati, per facilitare una maggiore continuità di assistenza rispetto a sistemi più frammentati.§§ Le strutture I/T/U sostengono anche la cura e l’educazione al diabete utilizzando infermieri della sanità pubblica e operatori sanitari della comunità per fornire assistenza e istruzione alla comunità.¶¶,***
Nel 1997, il Congresso ha istituito il Programma Speciale Diabete per gli Indiani (SDPI) (9). L’IFPD fornisce i finanziamenti necessari a 301 siti I/T/U per realizzare interventi che riducono i fattori di rischio per il diabete e le sue complicanze, tra cui l’ESRD-D(Tabella 2) (9).††† Inoltre, i fondi dello SDPI sono stati utilizzati dall’IHS per migliorare il suo programma nazionale per la diffusione di interventi basati sull’evidenza e per fornire formazione, strumenti per la raccolta e l’analisi dei dati e sostegno ai programmi per il diabete nelle comunità AI/AN di tutto il Paese. Grazie a SDPI, la partnership tra IHS e i programmi I/T/U è più forte e insieme forniscono un programma nazionale completo orientato alla salute pubblica che ha dimostrato di avere successo nell’affrontare l’epidemia di diabete e nel ridurre complicazioni come l’ESRD-D (9).
| Intervento | 1997 % | 2013 % |
|---|---|---|
| Squadre cliniche per il diabete | 30 | 96 |
| Registri dei pazienti diabetici | 34 | 98 |
| Servizi di nutrizione per adulti | 39 | 93 |
| Accesso ai dietisti registrati | 37 | 79 |
| Accesso agli specialisti dell’attività fisica | 8 | 74 |
| Accesso a materiale didattico sul diabete culturalmente personalizzato | 36 | 97 |
I risultati di questo rapporto sono soggetti ad almeno cinque limitazioni. In primo luogo, i dati si riferiscono alle persone che ricevono un trattamento ESRD come riportato al CMS e non includono i pazienti che hanno rifiutato il trattamento, quelli che sono morti prima di ricevere il trattamento, o quelli il cui trattamento non è stato riportato al CMS. In secondo luogo, la diagnosi primaria è stata ottenuta dal CMS Medical Evidence Report ed è stata basata sulla valutazione del paziente da parte di un medico, che potrebbe essere influenzata dalla consapevolezza del medico della prevalenza del diabete tra gli IA/AN. In terzo luogo, la classificazione differenziale della razza AI/AN nei sistemi di dati USRDS, U.S. Census, e IHS potrebbe portare a sovrastimare o sottostimare l’effettiva incidenza di ESRD-D in questa popolazione. In quarto luogo, i dati IHS sulla prevalenza del diabete potrebbero non essere rappresentativi della popolazione totale di AI/AN e potrebbero portare a una sovrastima o sottostima del numero di AI/AN con diabete negli Stati Uniti e, quindi, dell’incidenza dell’ESRD-D. Anche se queste distorsioni potrebbero aver influito sulle stime dell’incidenza, le tendenze dell’incidenza non sarebbero influenzate se le distorsioni rimanessero costanti nel tempo. Infine, i dati sulle misure del diabete riflettono l’assistenza fornita all’AI/AN che accede al sistema I/T/U e non possono essere generalizzati all’AI/AN che non lo fa.
L’ESRD-D è una condizione disabilitante e costosa associata ad un’elevata mortalità.§§§ La spesa Medicare per persona all’anno per i pazienti in emodialisi è stata di 84.550 dollari nel 2013, e il costo per persona all’anno per l’ESRD-D è stato di 82.141 dollari (1). Nel 2013, la spesa complessiva per l’ESRD-D è stata di 14 miliardi di dollari, circa la metà (45%) dei 31 miliardi di dollari di spesa complessiva per l’ESRD (1). Una diminuzione dell’incidenza dell’ESRD-D nella popolazione generale degli Stati Uniti paragonabile a quella della popolazione AI/AN potrebbe portare a un minor numero di casi di ESRD-D appena trattati e contribuire a livellare o a ridurre la spesa totale di Medicare per l’ESRD. L’integrazione di approcci basati sulla salute pubblica, clinici e comunitari per fornire interventi basati sull’evidenza, volti a ridurre i fattori di rischio ESRD-D, può sostenere e migliorare le tendenze nell’incidenza dell’ESRD-D.
References
- United States Renal Data System. 2015. Publisher Full Text
- CDC. 2014. Publisher Full Text
- ADVANCE Collaborative Group. Combined effects of routine blood pressure lowering and intensive glucose control on macrovascular and microvascular outcomes in patients with type 2 diabetes: new results from the ADVANCE trial.. Diabetes Care. 2009; 32:2068-74. DOI | PubMed
- RENAAL Study Investigators. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy.. N Engl J Med. 2001; 345:861-9. DOI | PubMed
- Patients with diagnosed diabetes mellitus can be accurately identified in an Indian Health Service patient registration database.. Public Health Rep. 2001; 116:45-50. DOI | PubMed
- Permutation tests for joinpoint regression with applications to cancer rates.. Stat Med. 2000; 19:335-51. DOI | PubMed
- National Cancer Institute. 2016. Publisher Full Text
- Clinical manifestations of kidney disease among US adults with diabetes, 1988–2014.. JAMA. 2016; 316:602-10. DOI | PubMed
- Indian Health Service.Publisher Full Text
- Indian Health Service.Publisher Full Text
- Racial and ethnic differences in trends of end-stage renal disease: United States, 1995 to 2005.. Adv Chronic Kidney Dis. 2008; 15:147-52. DOI | PubMed
- Diabetic nephropathy in American Indians, with a special emphasis on the Pima Indians.. Curr Diab Rep. 2008; 8:486-93. DOI | PubMed
- Improving diabetes care for American Indians.. Diabetes Care. 1993; 16:372-5. DOI | PubMed
- Reducing the burden of chronic kidney disease among American Indians.. Adv Chronic Kidney Dis. 2008; 15:168-73. DOI | PubMed
- A framework for public health action: the health impact pyramid.. Am J Public Health. 2010; 100:590-5. DOI | PubMed
- Caring for the patient with progressive renal disease.. IHS Prim Care Provid. 1990; 15:101-4.
- ADVANCE Collaborative Group. Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial.. Lancet. 2007; 370:829-40. DOI | PubMed
- Applying the diabetes quality improvement project indicators in the Indian Health Service primary care setting.. Diabetes Care. 2001; 24:22-6. DOI | PubMed
- Indian health service innovations have helped reduce health disparities affecting American Indian and Alaska native people.. Health Aff (Millwood). 2011; 30:1965-73. DOI | PubMed
Fonte
Bullock A, Burrows NR, Narva AS, Sheff K, Hora I, et al. (2017) Vital Signs: Decrease in Incidence of Diabetes-Related End-Stage Renal Disease among American Indians/Alaska Natives — United States, 1996–2013. MMWR. Morbidity and Mortality Weekly Report 66(1): . https://doi.org/10.15585/mmwr.mm6601e1





